نظرية الكم والذرة - الكيمياء 2 - ثاني ثانوي
القسم الأول
الفصل1: الحسابات الكيميائية
الفصل2: الإلكترونات في الذرات
الفصل3: الجدول الدوري والتدرج في خواص العناصر
الفصل4: المركبات الأيونية والفلزات
الفصل5: الروابط التساهمية
القسم الثاني
الفصل1: حالات المادة
الفصل2: الطاقة والتغيرات الكيميائية
الفصل3: سرعة التفاعلات الكيميائية
الفصل4: الاتزان الكيميائي
القسم الثالث
الفصل1: الهيدروكربونات
الفصل2: مشتقات المركبات الهيدروكربونية وتفاعلاتها
الفصل3: كيمياء الحياة (المركبات العضوية الحيوية)

نموذج بور للذرة
أهداف درس نظرية الكم والذرة
الشكل 1-10 يوضح ذرة تحتوي على إلكترون واحد
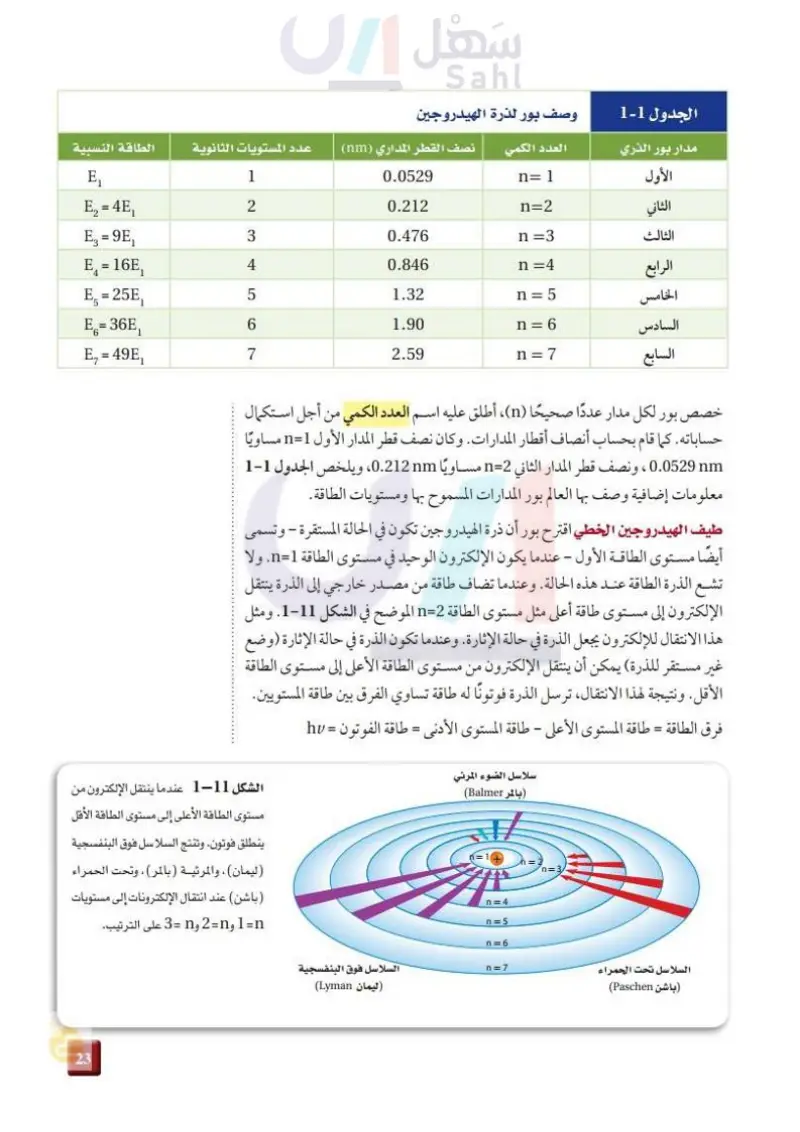
طاقة ذرة الهيدروجين
العدد الكمي
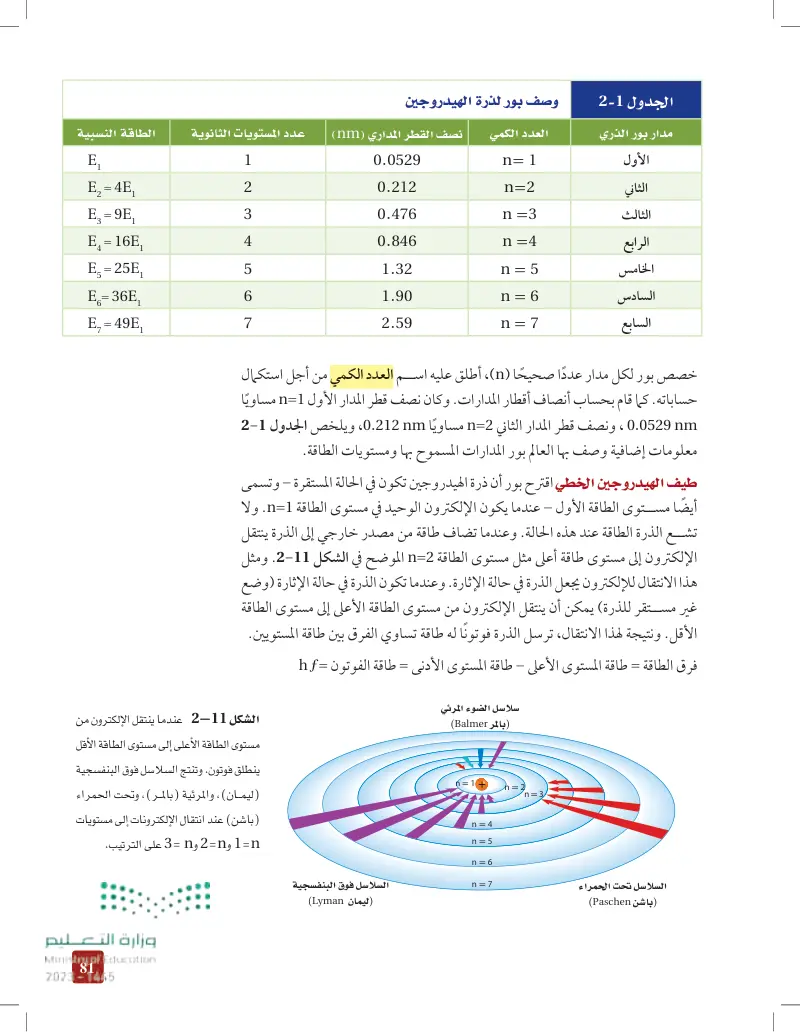
عندما ينتقل الإلكترون من مستوى الطاقة الأعلى إلى مستوى الطاقة الأقل ينطلق فوتون

مستويات الطاقة مشابهة لدرجات السلم

الإلكترونات موجات
العلاقة بين الجسم والموجة الكهرومغناطيسية

لماذا تتغير طاقة الفوتون؟
يعني مبدأ هايزنبرج للشك أيضا أنه من المستحيل تحديد مسارات ثابتة للإلكترونيات مثل المدارات الدائرية

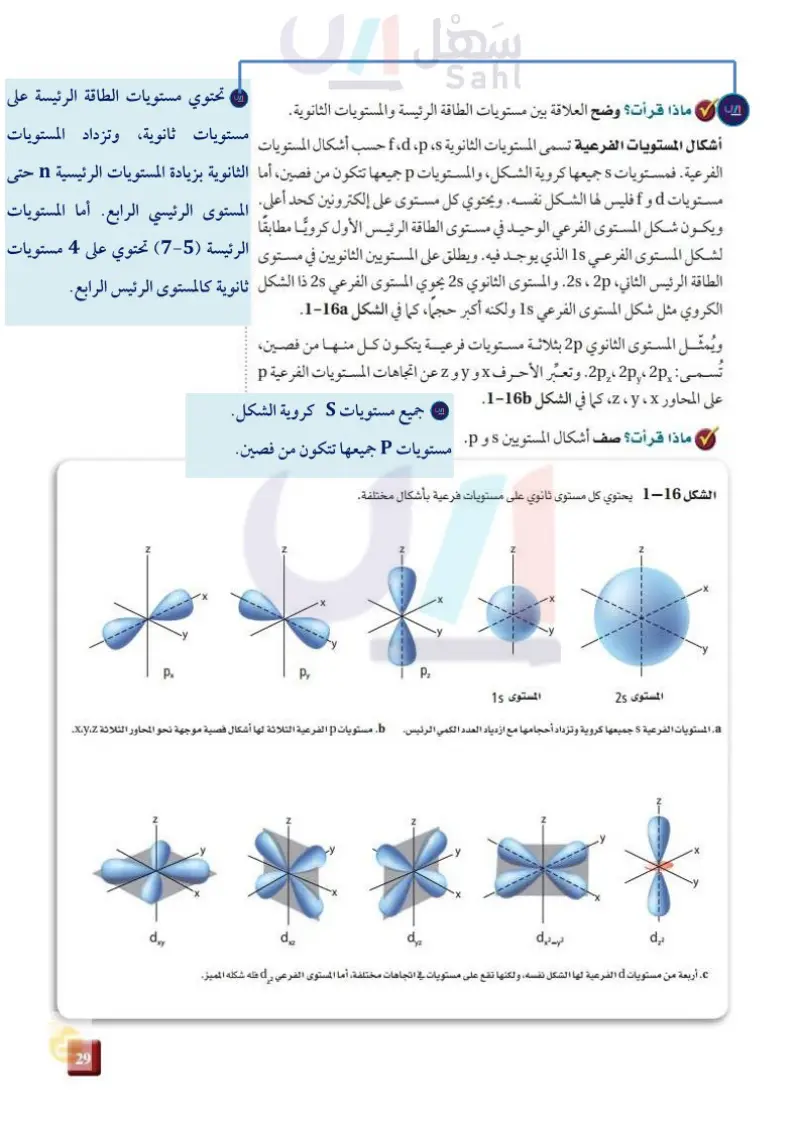
تمثل خريطة الكثافة احتمال وجود إلكترون في موقع معين حول النواة

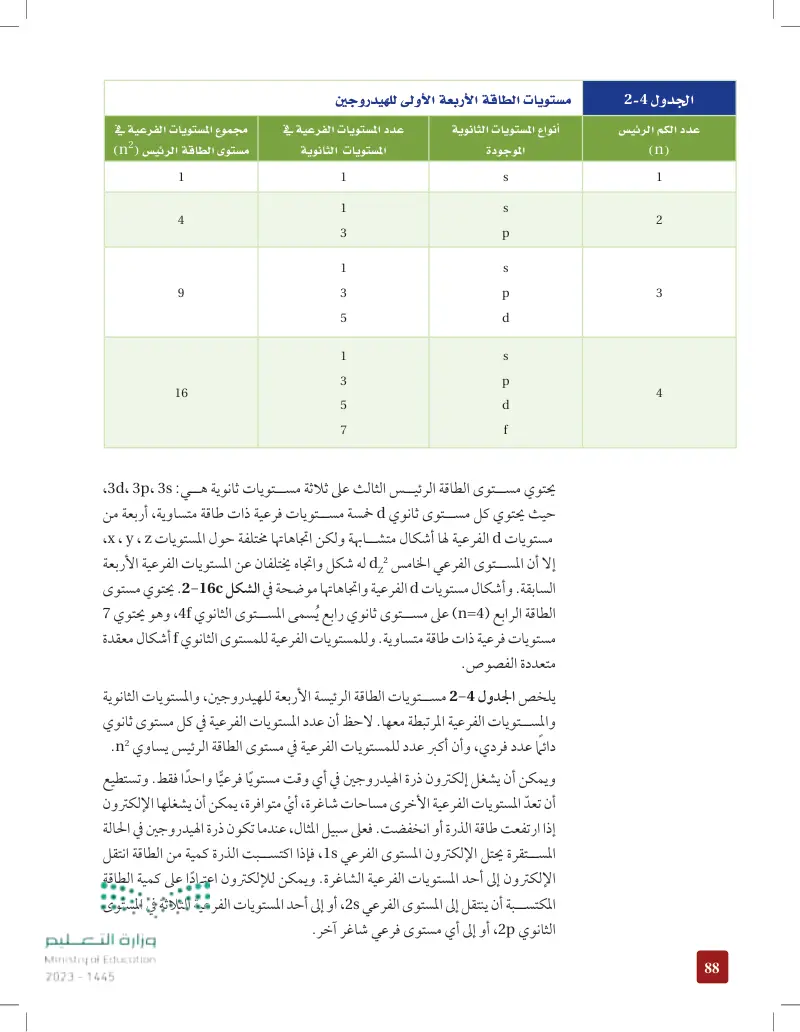
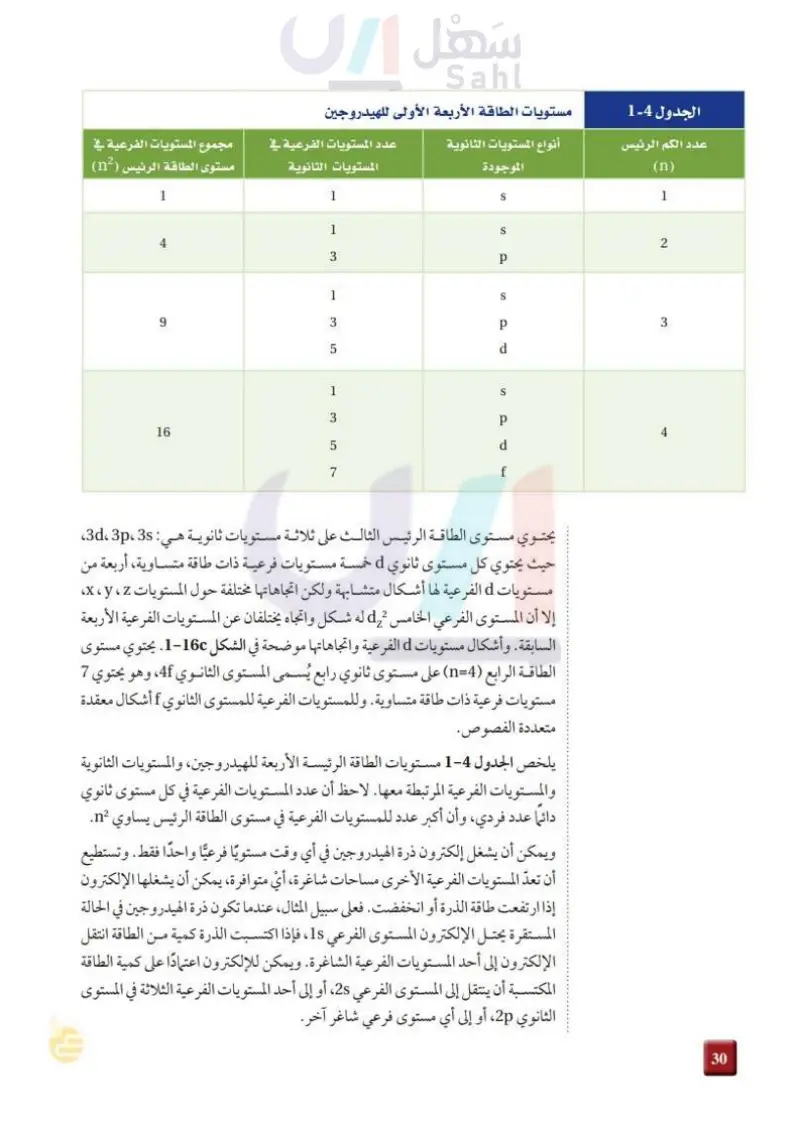
الجدول مستويات الطاقة الرئيسة
الجدول مستويات الطاقة الثانوية
عدد الكم الرئيسي


خلاصة درس نظرية الكم والذرة
احسب مستعينا بالمعلومات في الجدول 1-1 ، كم مرة يساوي نصف قطر مدار ذرة الهيدروجين السابع بالنسبة إلى نصف قطر مدارها الأول ، حسب نظرية بور ؟
فسر لماذا يكون موقع الإلكترون في ذرة غير معلوم بدقة . مستخدما مبدأ هايزنبرج للشـك والطبيعـة الموجية - الجسيمية ؟ وكيـف يعرف موقع الإلكترونات في الذرات ؟




Alkasir 555
منذ 3 سنوات
مافهمت حسبي الله عليكم
3  0
0 
 0
0 
الرجاء تسجيل الدخول لكتابة تعليق