الأكسدة والاختزال - الكيمياء 3 - ثالث ثانوي
الفصل1: المخاليط والمحاليل
الفصل2: الأحماض والقواعد
الفصل3: تفاعلات الأكسدة والاختزال
الفصل4: الكيمياء الكهربائية
مصادر تعليمية للطالب
تفاعلات الأكسدة والاختزال Redox Reactions وزارة التعليم Ministry of Education 2024-1446 2 31 الفكرة العامة تعد تفاعلات الأكسدة والاختزال من العمليات الكيميائية الشائعة في الطبيعة وفي الصناعة، وتتضمن انتقالًا للإلكترونات. 3-1 الأكسدة والاختزال الفكرة الرئيسة يعد تفاعلا الأكسدة والاختزال تفاعلين متكاملين؛ إذ تتأكسد ذرة وتختزل أخرى. 3-2 وزن معادلات الأكسدة والاختزال الفكرة الرئيسة تصبح معادلات الأكسدة والاختزال موزونة عندما تكون الزيادة الكلية في أعداد التأكسد مساوية للانخفاض الكلي في أعداد التأكسد للذرات الداخلة في التفاعل. حقائق كيميائية يمكن زيادة لمعان العصا الضوئية النشطة بتسخينها، لكن البريق لن يستمر طويلا. ليس بالضرورة أن يكون الضوء الناتج عن تفاعلات الأكسدة والاختزال مصحوبًا بالحرارة. يستعمل نحو 90% تقريبًا من الأحياء البحرية شكلًا من أشكال الضوء الحيوي الذي يتولّد من تفاعلات الأكسدة والاختزال. عصا ضوئية وعاء زجاجي من H2O2 102

تفاعلات الأكسدة والاختزال من العمليات الكيميائية الشائعة في الطبيعة وفي الصناعة وتتضمن انتقالا للإلكترونات
يمكن زيادة لمـعان العصا الضـوئية النشطة بتسخينها لكن البريق لن يستمر طويلا
نشاطات تمهيدية تجربة استهلالية ماذا يحدث عندما يتفاعل الحديد وكبريتات النحاس II ؟ ينتج الصدأ عندما يتفاعل الحديد والأكسجين، ويتفاعل الحديد أيضًا مع مواد أخرى غير الأكسجين. المطويات وزن معادلات الأكسدة منظمات الأفكار والاختزال صمّم المطوية الآتية لتساعدك على تلخيص المعلومات حول الطرائق خطوات العمل BES اقرأ نموذج احتياطات السلامة في المختبر. 2 استعمل قطعةً من ورق الصنفرة لتلميع مسمار الحديد. .3. أضف 3mL تقريبًا من محلول 1.0M من كبريتات النحاس CuSO II إلى أنبوب اختبار، وضع المسمار الذي جری تلميعه في محلول CuSO، ثم ضع أنبوب الاختبار في حامل الأنابيب، وراقبه مدة 10 دقائق ، ثم سجل ملاحظاتك. تحليل النتائج 4 .1 فسّر ما يحدث للون محلول كبريتات النحاس. 2 حدد المادة التي التصقت بالمسمار. 3. اكتب المعادلة الكيميائية الموزونة لهذا التفاعل. استقصاء ماذا يمكن أن يحدث للنحاس لو وضع في محلول كبريتات الحديد؟ صمّم تجربةً لاختبار فرضيتك. المختلفة في وزن معادلات الأكسدة والاختزال. الخطوة 1 اجمع طبقتين من الورق، واجعل طرف الورقة العلوية على بعد 2cm من حافة الورقة السفلية كما في الشكل. الخطوة 2 اثن الحواف السفلية إلى أعلى لتكوّن أربعة تفرعات متساوية. ثم ثبّت الثنية بالضغط عليها لتحافظ على التفرع في مكانه جيدًا، كما في الشكل المجاور. الخطوة 3 ثبت الثنيات أنصاف التفاعل معادلة الأكسدة والاختزال الأيونية الكلية طريقة عدد التأكسد . وزن معادلات الأكسدة والاختزال وعنونها على النحو الآتي: وزن معادلات الأكسدة ،والاختزال، طريقة عدد التأكسد، معادلة الأكسدة والاختزال الأيونية الكلية، أنصاف التفاعل. المطويات استعمل المطوية في القسم 2-3 ولخص ما تقرؤه حول موازنة معادلات الأكسدة والاختزال، واعرض مثالا على كل طريقة. 103 وزاره ليم Ministry of Education 2024-1446

صمم المطوية الآتية لتساعدك على تلخيص المعلومات حول الطرائق المختلفة في وزن معادلات الأكسدة والاختزال
رابط الدرس الرقمي www.ien.edu.sa 3-1 الأهداف الأكسدة والاختزال تصف تفاعلات الأكسدة والاختزال Oxidation and Reduction تحدّد العوامل المؤكسدة والمختزلة. تحدد عدد التأكسد لعنصر في مركب. الفكرة الرئيسة يُعدّ تفاعلا الأكسدة والاختزال تفاعلين متكاملين؛ إذ تتأكسد ذرة وتختزل أخرى. تفسر تفاعلات الأكسدة والاختزال الربط مع الحياة ينتج ضوء العصا الضوئية عن تفاعل كيميائي، فعندما تكسر الكبسولة من حيث التغير في حالة التأكسد الزجاجية داخل الإطار البلاستيكي يحدث تفاعل بين مادتين، وتنتقل الإلكترونات، مراجعة المفردات فتتحول الطاقة الكيميائية إلى طاقة ضوئية. انتقال الإلكترون وتفاعل الأكسدة والاختزال الأيون المتفرّج الأيون غير Electron Transfer and Redox Reactions المعادلة الأيونية. المشترك في التفاعل ولا يظهر في يمكن تصنيف التفاعلات الكيميائية في العادة إلى خمسة أنواع من التفاعلات هي: التكوين، التفكك، والاحتراق، والإحلال البسيط، والإحلال المزدوج. ومن خواص تفاعلات الاحتراق والإحلال البسيط أنهما يتضمنان انتقال الإلكترونات من ذرة إلى أخرى، كما المفردات الجديدة هو الحال في كثير من تفاعلات التكوين و التفكك. ففي تفاعل التكوين على سبيل المثال، تفاعل الأكسدة والاختزال يتفاعل الصوديوم Na ، والكلور Cl لتكوين المركب الأيوني NaCl، وينتقل إلكترونان من ذرتي صوديوم إلى جزيء الكلور ويتكون أيونان من الصوديوم وأيونان من الكلوريد، وتكون المعادلة الكيميائية لهذا التفاعل على النحو الآتي: الأكسدة الاختزال 2Na(s) + Cl2(g) → 2NaCl(s) العامل المؤكسد المعادلة الكيميائية الكاملة : العامل المختزل والمعادلة الأيونية الكلية (الأيونات المكونة للبلورة) 2Na(s) + Cl2(g) → 2Na+ (s) + 2C1- (s) أما تفاعل الماغنسيوم في الهواء الذي يتضمن انتقال الإلكترونات فهو مثال على تفاعل الاحتراق. المعادلة الكيميائية الكاملة : المعادلة الأيونية الكلية (الأيونات المكونة للبلورة) -> 2Mg(s) + O2(g) → 2MgO (s) 2Mg(s) + O2(g) 2Mg2+ (s) + 202-( (s) →> عندما يتفاعل الماغنسيوم مع الأكسجين، كما في الشكل 1-3، فإنّ كلّ ذرة ماغنسيوم تعطي إلكترونين إلى كل ذرة أكسجين، وتتحول ذرة الماغنسيوم إلى أيون Mg، وتتحول وزارة التعليم Ministry of Education 2024-1446 N 2Mg(s) تفقد كل منهما إلكترونين 2e- + + 2e 02(g) تكتسب كل منهما إلكترونين ↑ 2MgO (s) 2+ 2- 2+ 2- الشكل 1-3 يتضمن تفاعل الماغنسيوم مع الأكسجين انتقال الإلكترونات من الماغنسيوم إلى الأكسجين؛ لذا فإن هذا التفاعل هو تفاعل أكسدة واختزال. صنّف التفاعل بين الماغنسيوم والأكسجين. 104

أهداف درس الأكسدة والاختزال
2Br- + Clz → Br2 + 2CI- تكتسب كل منهما إلكترونا e يفقد إلكترونا يفقد إلكترونا الشكل 2-3 التفاعل بين محلول أيونات البروميد وغاز الكلور هو تفاعل أكسدة ، هنا تنتقل الإلكترونات من أيونات البروم إلى الكلور. ذرة الأكسجين إلى الأيون 02 ، ويُسمى التفاعل الذي انتقلت فيه الإلكترونات من إحدى الذرات إلى ذرة أخرى تفاعل الأكسدة والاختزال. لنأخذ تفاعل الإحلال البسيط بين المحلول المائي للكلور وأيونات البروميد لتكوين محلول مائي من كلوريد البوتاسيوم والبروم الموضح في الشكل 32 المعادلة الكيميائية الكاملة : المعادلة الكلية : 2KBr(aq) +Cl2(aq) → 2KCl(aq) +Br2(aq) 2Br¯ (aq) +Cl2(aq) → Br2(aq) +2Cl(aq) المفردات. أصل الكلمة يُلاحظ أن الكلور يكتسب الإلكترونات من أيونات البروميد ليكون أيونات الكلوريد، الاختزال (Reduction) وعندما يفقد أيونا البروميد الإلكترونات تتحد ذرتا البروم برابطة تساهمية لتكوين جزيء جاءت من الأصل اللاتيني Bra. إن تكوين الرابطة التساهمية بمشاركة الإلكترونات هو أيضًا تفاعل أكسدة واختزال. الأكسدة والاختزال أطلقت كلمة الأكسدة فيما مضى على التفاعلات التي تتضمن اتحاد المادة بالأكسجين، أما الآن فتعرّف عملية الأكسدة على أنها فقدان ذرة المادة للإلكترونات. تفحص مرةً أخرى معادلة تفاعل الصوديوم والكلور الكلية، تلاحظ أن الصوديوم قد تأكسد لأنه فقد إلكترونا. التأكسد: Na → Na+ + e- وحتى يحدث تفاعل الأكسدة يجب أن تُكتسب الإلكترونات التي تفقدها المادة المتأكسدة من قبل ذرات أو أيونات مادة أخرى، وبعبارة أخرى يجب أن تكون هناك عملية مرافقة تتضمن اكتساب الإلكترونات المفقودة . أما عملية الاختزال فتعرّف على أنها اكتساب ذرات المادة للإلكترونات. وبالرجوع إلى مثال كلوريد الصوديوم فإن تفاعل الاختزال المرافق لتفاعل الأكسدة هو اختزال الكلور. الاختزال: Cl + 2e- 2Cl- -> إذن فالأكسدة والاختزال عمليتان مترافقتان متكاملتان؛ فلا يحدث تفاعل الأكسدة إلا إذا حدث تفاعل اختزال، ومن المهم جدًّا التمييز بين تفاعلي الأكسدة والاختزال. re، وتعني الخلف، وducere وتعني يقود. 105 وزار سليم Ministry of Education 2024-1446

أًل الكلمة الاختزال
CI- كلوريد البوتاسيوم (صلب) K+ الكلور ( غاز) الشكل -3-3 يتفاعل كل من فلز البوتاسيوم وغاز الكلور تفاعل أكسدة واختزال لتكوين كلوريد البوتاسيوم. البوتاسيوم (صلب) مهن في الكيمياء التغير في عدد التأكسد تتذكر أن عدد التأكسد لذرة في المركب الأيوني هو عدد الإلكترونات التي فقدتها أو اكتسبتها الذرة عندما كوّنت الأيونات، وأن تفاعل البوتاسيوم مع الكلور الموضح في الشكل ،33، هو تفاعل أكسدة واختزال، ومعادلة تفاعل فلز البوتاسيوم مع غاز الكلور هي على النحو الآتي: المعادلة الكيميائية الكاملة : (2K(s) + Cl2(g) + 2KCl(s 2K (s) + Cl2(g) → 2K+ المعادلة الأيونية الكلية : (2K(s) + 2CI (s → صانع الفخار فنان يصنع يوجد البوتاسيوم ضمن عناصر المجموعة الأولى في الجدول الدوري، التي تميل إلى الفخار، ويستعمل مواد تحتوي فقد إلكترون واحد في التفاعل؛ بسبب انخفاض كهروسالبيتها، وعدد تأكسدها 1+ على أيونات فلزية لإضفاء ومن ناحية أخرى يوجد الكلور ضمن عناصر المجموعة 17 التي تميل إلى اكتساب الألوان المختلفة على الفخار الإلكترونات؛ لأن كهروسالبيتها عالية، وعدد تأكسدها في كثير من المركبات 1-. ففي عند حرقه وتظهر المواد مفهوم الأكسدة والاختزال يمكنك القول إن ذرات البوتاسيوم قد تأكسدت من حالة الزجاجية، التي تحتوي على الصفر إلى حالة 1 ؛ لأن كل ذرة فقدت إلكتروناً، واختزلت ذرات الكلور من الصفر إلى الحالة ، فكل ذرة أو أيون عند اختزاله يقل عدد تأكسده. وعلى العكس من ذلك المائل إلى الزرقة عند تأكسدها عندما تتأكسد ذرة أو أيون يزيد عدد تأكسدها. وتعطي اللون الأحمر عند حرقها أيونات النحاس، باللون الأخضر 106 في الفرن. ويعد عدد التأكسد أداةً يستعملها العلماء لكتابة المعادلة الكيميائية لمساعدتهم على الاحتفاظ بمسار حركة الإلكترونات في تفاعل الأكسدة. ويكتب عدد التأكسد مع الإشارة السالبة أو الموجبة قبل العدد 2 ، 3 ، في حين تُكتب إشارة الشحنة الأيونية بعد العدد 2 ، 3). عدد التأكسد : 3 الشحنة الأيونية : 3 6 ماذا قرأت؟ حدّد أي العناصر أكثر قابليةً لاكتساب الإلكترونات البوتاسيوم أم الكلور ؟ وزارة التعليم Ministry of Education 2024-1446

يتفاعل كل من فلز البوتاسيوم وغاز الكلور تفاعل أكسدة واختزال لتكوين كلوريد البوتاسيوم
أي العناصر أكثر قابلية لاكتساب الإلكترونات: البوتاسيوم أم الكلور
مهن في الكيمياء صانع الفخار
العوامل المؤكسدة والعوامل المختزلة Oxidizing and Reducing Agents الجدول ملخص تفاعلات الأكسدة والاختزال 3-1 يمكن وصف تفاعل البوتاسيوم – الكلور في الشكل 3-3 بأن البوتاسيوم قد تأكسد بواسطة الكلور. المادة التي يحدث لها اختزال (تكتسب إلكترونات) تُسمى عاملا مؤكسدًا، أما المادة التي يحدث لها أكسدة (تفقد إلكترونات) فتُسمى عاملا مختزلا؛ لذا فالعامل المختزل في تفاعل البوتاسيوم – الكلور هو البوتاسيوم؛ أي المادة التي تأكسدت. أكسدة العملية الأكسدة تفقد إلكترونا. 2K (s) + Cl2(g) → 2KCl(s) e انتقال الإلكترونات X المادة المتفاعلة . X يفقد إلكترونًا. يتأكسد العامل . X عامل مختزل اختزال العامل المختزل : K العامل المؤكسد : Cle المختزل. ويتأكسد. و من التطبيقات الشائعة على تفاعلات الأكسدة والاختزال إزالة الشوائب من يزيد عدد التأكسد. يزيد عدد التأكسد للمادة X. و الاختزال الفلزات. وتُعدَّ العوامل المؤكسدة والمختزلة الأخرى مفيدة في الحياة اليومية. المادة المتفاعلة • Y يكتسب إلكترونًا. فعلى سبيل المثال عند إضافة مبيض الغسيل إلى الملابس لتبييضها، فإنك الأخرى تكتسب تستعمل محلولاً من هيبوكلوريت الصوديوم NaClO؛ وهو عامل مؤكسد يؤدي إلى أكسدة البقع والأصباغ ومواد أخرى. ويلخص الجدول 1-3 الطرائق المختلفة لوصف تفاعلات الأكسدة والاختزال. إلكترونا. يختزل العامل المؤكسد. . يقلّ. يقل عدد التأكسد. . Y العامل المؤكسد يُختزل. يقل عدد التأكسد للمادة Y. ملاحظة تفاعل الأكسدة والاختزال كيف يمكن إزالة الشوائب من الفضة؟ الخطوات BOPS 1. اقرأ نموذج الأمان في المختبر. 6. أمسك الكأس بالماسك وضعها على السخان، وسخّن محتوياتها حتى درجة الغليان، مع الحفاظ على الحرارة مدة 15 دقيقة تقريبًا حتى تزول الشوائب. التحليل 1. اكتب معادلة تفاعل الفضة مع كبريتيد الهيدروجين، التي تنتج 2 مع قطعةً من رقائق الألومنيوم برفق مستعملا الصوف لإزالة كبريتيد الفضة والهيدروجين. أي طبقة مؤكسدة تغطيها. 2. اكتب معادلة تفاعل كبريتيد الفضة (الشوائب) مع رقائق 3. لف قطعة صغيرة متأكسدة من معدن الفضة برقائق الألومنيوم والتي تنتج كبريتيد الألومنيوم والفضة. الألومنيوم ، وتأكد من التصاق المنطقة المتأكسدة تمامًا برقائق 3 حدّد أي الفلزات أكثر نشاطًا : الألومنيوم أم الفضة؟ وكيف تعرف الألومنيوم. ذلك من النتائج؟ مصنوعة من الفضة؟ 4. ضع القطعة الملفوفة في كأس سعتها 400mL ، وأضف كميةً .4 فسر لماذا يجب ألا تستعمل أواني الألومنيوم عند تنظيف مواد محددةً من ماء الصنبور حتى تغطيها تمامًا. 5. أضف مقدار ملعقة من صودا الخبز، ومقدار ملعقة من ملح المائدة إلى الكأس. 107 وزار سليم Ministry of Education 2024-1446

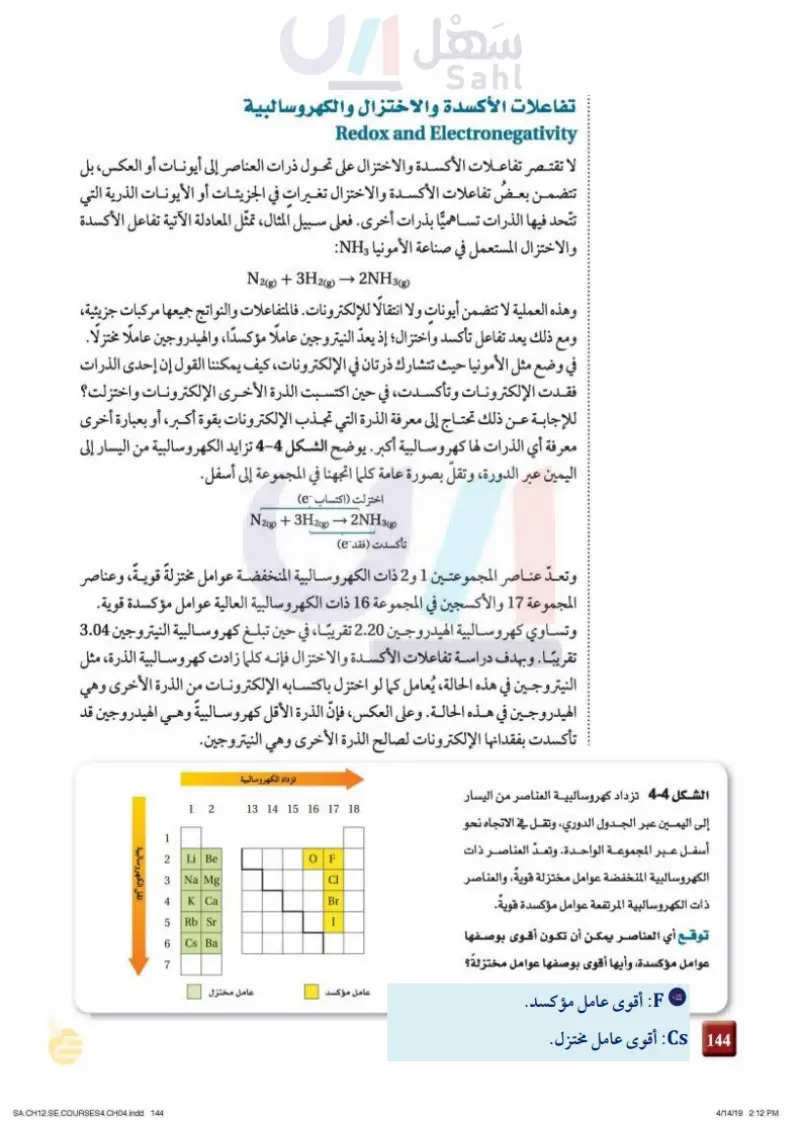
تفاعلات الأكسدة والاختزال والكهروسالبية Redox and Electronegativity لا تقتصر تفاعلات الأكسدة والاختزال على تحول ذرات العناصر إلى أيونات أو العكس، بل تتضمن بعضُ تفاعلات الأكسدة والاختزال تغيرات في الجزيئات أو الأيونات الذرية التي تتحد فيها الذرات تساهميَّا بذرات أخرى. فعلى سبيل المثال، تمثل المعادلة الآتية تفاعل الأكسدة والاختزال المستعمل في صناعة الأمونيا NH 2NH3(g) N2(g) + 3H2(g) وهذه العملية لا تتضمن أيونات ولا انتقالًا للإلكترونات. فالمتفاعلات والنواتج جميعها مركبات جزيئية، ومع ذلك يعد تفاعل تأكسد واختزال؛ إذ يعد النيتروجين عاملا مؤكسدا، والهيدروجين عاملا مختزلا. في وضع مثل الأمونيا حيث تتشارك ذرتان في الإلكترونات، كيف يمكننا القول إن إحدى الذرات فقدت الإلكترونات وتأكسدت، في حين اكتسبت الذرة الأخرى الإلكترونات واختزلت؟ للإجابة عن ذلك تحتاج إلى معرفة الذرة التي تجذب الإلكترونات بقوة أكبر، أو بعبارة أخرى معرفة أي الذرات لها كهروسالبية أكبر . يوضح الشكل -- تزايد الكهروسالبية من اليسار إلى اليمين عبر الدورة، وتقل بصورة عامة كلما اتجهنا في المجموعة إلى أسفل. اختزلت اکتساب -e) N2(g) + 3H2(g) →> 2NH3(g) تأكسدت (فقد e) وتعد عناصر المجموعتين 1 و2 ذات الكهروسالبية المنخفضة عوامل مختزلة قوية، وعناصر المجموعة 17 والأكسجين في المجموعة 16 ذات الكهروسالبية العالية عوامل مؤكسدة قوية. وتساوي كهروسالبية الهيدروجين 2.20 تقريبًا، في حين تبلغ كهروسالبية النيتروجين 3.04 تقريبًا. وبهدف دراسة تفاعلات الأكسدة والاختزال فإنه كلما زادت كهروسالبية الذرة، مثل النيتروجين في هذه الحالة، يُعامل كما لو اختزل باكتسابه الإلكترونات من الذرة الأخرى وهي الهيدروجين في هذه الحالة. وعلى العكس، فإنّ الذرة الأقل كهروسالبية وهي الهيدروجين قد تأكسدت بفقدانها الإلكترونات لصالح الذرة الأخرى وهي النيتروجين. الشكل -4-3 تزداد كهروسالبية العناصر من اليسار إلى اليمين عبر الجدول الدوري، وتقل في الاتجاه نحو أسفل عبر المجموعة الواحدة. وتعد العناصر ذات الكهروسالبية المنخفضة عوامل مختزلة قويةً، والعناصر ذات الكهروسالبية المرتفعة عوامل مؤكسدة قويةً. توقع أي العناصر يمكن أن تكون أقوى بوصفها عوامل مؤكسدة، وأيها أقوى بوصفها عوامل مختزلة؟ . تزداد الكهروسالبية تقل الكهروسالبية وزارة التعليم Ministry of Education 2024-1446 108

مثال 1-3 تفاعلات الأكسدة والاختزال تمثل المعادلة الآتية تفاعل أكسدة واختزال واقع الكيمياء في الحياة الألومنيوم والحديد. 2A1 + 2Fe3+ + 302 → 2Fe + 2Al3+ + 302- حدد المادة التي تأكسدت والمادة التي اختزلت في هذا التفاعل. حدّد العامل المؤكسد والعامل المختزل. 1 تحليل المسألة و لقد أعطيت المتفاعلات والنواتج في التفاعل، لذا عليك تحديد انتقال الإلكترونات ،الحاصل، ثم يمكنك تطبيق تعريف العامل المؤكسد والعامل المختزل للإجابة عن السؤال. 2 حساب المطلوب حدّد عمليتي التأكسد والاختزال. فقد الألومنيوم 3 إلكترونات (فقدان الإلكترونات - أكسدة ) - Al → Al3 + + 3e وأصبح أيون الألومنيوم. اكتسب الحديد 3 إلكترونات اكتساب الإلكترونات - اختزال) Fe3+ + 3e - → Fe فقدها الألومنيوم. الأكسدة الصدأ يتأكسد الحديد عندما يلامسه الهواء الرطب، مكونا أكسيد الحديد III لأن الألومنيوم تأكسد لذا فهو العامل المختزل، ولأن الحديد اختزل لذا فهو العامل Fe2O3 ويسمى الصدأ، والصدأ شائع جدا؛ لأن مركبات الحديد سريعة التفاعل مع الأكسجين، والحديد النقي غير شائع المؤكسد. 83 تقويم الإجابة تأكسد الألومنيوم في هذه العملية بفقده الإلكترونات، في حين اختزل الحديد في الطبيعة. وحاليًا يستعمل الفولاذ وهو واكتسب الإلكترونات، ومن ثَمّ يتفق تعريف كل من الأكسدة والاختزال والعامل سبيكة يعدّ الحديد المكون الأساسي لها. المؤكسد والعامل المختزل مع ما تقدم لاحظ أن عدد تأكسد الأكسجين لم يتغير في وهناك طرائق كثيرة يمكن اتباعها لحماية هذا التفاعل ؛ لذا لا يعد الأكسجين عاملا مفتاحيًا لحل المسألة. مسائل تدريبية الحديد كالطلاء، والدهان، وإضافة المواد البلاستيكية لحماية منتجات 1. حدّد التغيرات، في كل مما يلي سواء أكانت أكسدة أم اختزالا؟ وتذكر أن – e هو رمز الإلكترون: الحديد من الأكسدة. 109 وزار سليم Ministry of Education 2024-1446 Fe2+ → Fe3+ + e c Ag+ + e- →→ Ag.d I2 + 2e- → 2 - .a K → K+ + e- .b 2 حدّد العناصر التي تأكسدت والعناصر التي اختزلت في العمليات الآتية: 2Br- + Cl2→ Br2 + 2Cl- .a 2Ce + 3Cu2+ + 3Cu + 2Ce3+ .b 2Zn + O22ZnO .c 2Na + 2H+ → 2Na+ + H2 .d .3 حدّد العامل المؤكسد والعامل المختزل في التفاعل الآتي: Fe(s) + 2Ag+(aq) → Fe²+ (aq) + 2Ag(s) .4. تحفيز حدّد العامل المؤكسد والعامل المختزل في التفاعل الآتي: Mg(s) + I2(s) → MgI2(s) .a H2S (g) + Cl2(g) → S(s) + 2HCl (g) .b

الاكسدة
تجربة عملية 106 الشكل 5-3 صخر يوضح طبقات من الحديد ناتجة عن الاختلاف في حالة تأكسد الحديد. ميل الفلزات إلى فقد الإلكترونات ارجع إلى دليل التجارب العملية على منصة عين الإثرائية تحديد أعداد التأكسد Determining Oxidation Numbers لنفهم جميع أنواع تفاعلات الأكسدة والاختزال لا بد من تعرف الطريقة التي يتم بها تحديد عدد التأكسد (n) لذرات العناصر الداخلة في التفاعل، ويلخص الجدول 2-3 القواعد التي يستعملها الكيميائيون لتسهيل عملية التحديد. لاحظ أن الجدول لا يتضمن العناصر الانتقالية وأشباه الفلزات واللافلزات التي قد يكون لها أكثر من عدد تأكسد في المركبات المختلفة. فعلى سبيل المثال للحديد أعداد تأكسد مختلفة يُستدل عليها من خلال الألوان الموضحة في الشكل .35 الجدول 2-3 قواعد تحديد أعداد التأكسد للعناصر القاعدة 1. عدد تأكسد الذرة غير المتحدة يساوي صفرًا. 2 عدد تأكسد الأيون الأحادي الذرة يساوي شحنة الأيون. مثال Na, O2, Cl2, 2 Ca2+ Br- 3 عدد تأكسد الذرة الأكثر كهروسالبية في الجزيء N في NH3 أو الأيون المعقد هو الشحنة نفسها التي سيكون عليها كما لو كان أيونا. 4 عدد تأكسد العنصر الأكثر كهروسالبية (الفلور) هو دائما 1- عندما يرتبط بعنصر آخر. 5 عدد تأكسد الأكسجين في المركب دائما يساوي 0 في NO F في LiF في NO2 2- ما عدا مركبات فوق الأكاسيد كما في المركب فوق أكسيد الهيدروجين H2O2، حيث يساوي في H2O2 1- . وعندما يرتبط بالفلور العنصر الوحيد الذي له كهروسالبية أعلى من الأكسجين يكون عدد في OF2 تأكسده موجبًا. 6 عدد تأكسد الهيدروجين في معظم مركباته يساوي 1+ ماعدا الهيدريدات فيساوي 1- 7 عدد تأكسد فلزات المجموعتين الأولى والثانية والألومنيوم يساوي عدد إلكترونات المدار الخارجي. .8 8 مجموع أعداد التأكسد في المركبات المتعادلة يساوي صفرًا. 9. مجموع أعداد التأكسد للمجموعات الذرية يساوي شحنة المجموعة. H في NaH عدد التأكسد (1) 0 +2 −1 -3 -2 −1 -2 −1 +2 -1 +1 K +2 Ca +3 Al (+2)+2(-1) = 0 CaBr2 (+4)+3(-2)=-2 SO2- وزارة التعليم Ministry of Education 2024-1446 110

صخر يوضح طبقات من الحديد ناتجة عن الاختلاف في حالة تأكسد الحديد
ميل الفلزات إلى فقد الإلكترونات
مثال 2-3 تحديد أعداد التأكسد استعمل قواعد تحديد أعداد التأكسد لحساب عدد التأكسد لكل عنصر في مركب كلورات البوتاسيوم KCIO3 وفي أيون الكبريتيت SO. تحليل المسألة أُعطيت أعداد التأكسد في قواعد تحديد أعداد التأكسد لكل من الأكسجين والبوتاسيوم، وأُعطيت الشحنة الكلية للأيون أو المركب. استخدم هذه المعلومات، وطبّق القواعد، وحدّد عدد التأكسد لكل من الكلور والكبريت (اجعل n عدد التأكسد للعنصر في السؤال. المطلوب na = ? ns = ? المعطيات KClO3 SO32- no = -2 nx = +1 B حساب المطلوب بين أعداد التأكسد لكل من العناصر المعروفة، واجعل مجموع أعداد التأكسد للعناصر في المركب أو الأيون مساويةً للصفر أو لشحنة الأيون، ثم جد القيمة المجهولة من أعداد التأكسد. مجموع أعداد التأكسد للمركب المتعادل هو صفر. ولفلزات المجموعة الأولى يكون 1+ = n. عوّض 2 = nx = + 1. no جد قيمة nca. مجموع أعداد التأكسد للأيون المتعدد الذرات يساوي شحنة الأيون. عوض 2- = no = (nx) + (na) + 3 (no) = 0 (+1) + (na) +3(-2) = 0 1 + na + (6) = 0 na = +5 (ns) + 3 (no) = −2 (ns) + 3(-2) = −2 : ns + (6) = -2 ns = +4 جد قيمة ns. 3 تقويم الإجابة و لقد طبقت قواعد حساب أعداد التأكسد تطبيقًا صحيحًا. فجميع أعداد التأكسد لكل عنصر أخذت القيمة الصحيحة لها. مسائل تدريبية 5 حدّد عدد التأكسد للعنصر المكتوب بلون داكن في الصيغ الجزيئية الآتية: NaClO4 .a AlPO4 .b HNO2 .C 6. حدد عدد التأكسد للعنصر المكتوب بلون داكن في صيغ الأيونات الآتية: NH4+ .a AsO43- .b 7 حدّد عدد التأكسد للنيتروجين في الجزيئات الآتية: NH3 .a KCN .c CrO42- N2H4 c 8. تحفيز حدّد التغير الكلي في عدد تأكسد كل من العناصر في معادلات الأكسدة والاختزال الآتية: 111 وزارف ليم Ministry of Education 2024-1446 C(s) + O2(g) → CO2 (g) .a Cl2(g) + ZnI2(s) → ZnCl2(s) + I2(s) .b Cdo (s) + CO(g) →> Cd(s) + CO2(g) .c

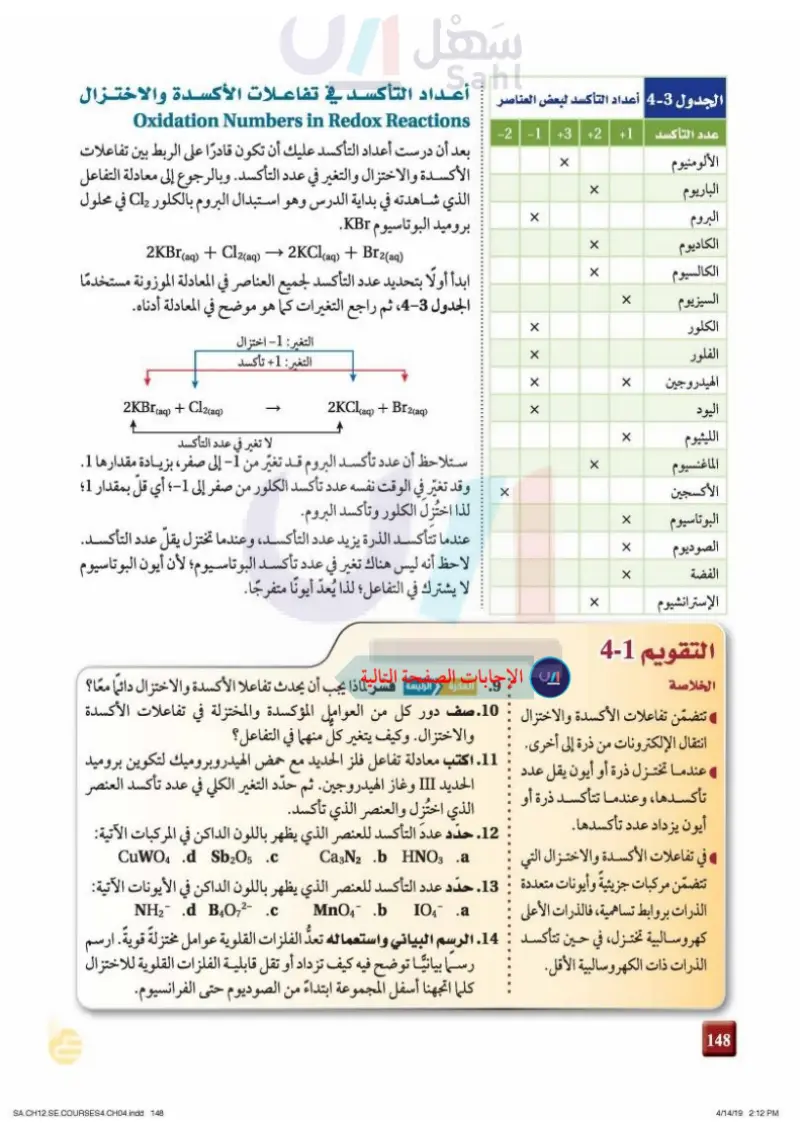
الجدول - أعداد التأكسد لبعض العناصر أعداد التأكسد في تفاعلات الأكسدة والاختزال عدد التأكسد الألومنيوم الباريوم البروم الكاديوم الكالسيوم السيزيوم الكلور الفلور الهيدروجين -2-1 +3 +2 +1 X X xx X X ☑ X X X Oxidation Numbers in Redox Reactions بعد أن درست أعداد التأكسد عليك أن تكون قادرًا على الربط بين تفاعلات الأكسدة والاختزال والتغير في عدد التأكسد وبالرجوع إلى معادلة التفاعل الذي شاهدته في بداية الدرس وهو استبدال البروم بالكلور Cle في محلول بروميد البوتاسيوم KBr. → 2KCl(aq) + Br2(aq) 2KBr(aq) + Cl2(aq) ابدأ أولًا بتحديد عدد التأكسد لجميع العناصر في المعادلة الموزونة مستخدمًا الجدول 3-3 ، ثم راجع التغيرات كما هو موضح في المعادلة أدناه. X 2KCl(aq) + Br2(aq) X A التغير: 1- اختزال التغير: 1+ تأكسد 2KBr(aq) + Cl2(aq) لا تغير في عدد التأكسد ستلاحظ أن عدد تأكسد البروم قد تغيّر من 1 إلى صفر، بزيادة مقدارها 1. وقد تغيّر في الوقت نفسه عدد تأكسد الكلور من صفر إلى 1؛ أي قل بمقدار 1؛ لذا اختزل الكلور وتأكسد البروم. عندما تتأكسد الذرة يزيد عدد التأكسد، وعندما تختزل يقل عدد التأكسد. لاحظ أنه ليس هناك تغير في عدد تأكسد البوتاسيوم؛ لأن أيون البوتاسيوم لا يشترك في التفاعل ؛ لذا يُعدّ أيونا متفرجًا. X ☑ X X X ☑ ☑ اليود الليثيوم الماغنسيوم الأكسجين البوتاسيوم الصوديوم الفضة الإسترانشيوم التقويم 1-3 الخلاصة .9 الفكرة الرئيسة فسّر لماذا يجب أن يحدث تفاعلا الأكسدة والاختزال دائما معا ؟ تتضمن تفاعلات الأكسدة والاختزال 10. صف دور كل من العوامل المؤكسدة والمختزلة في تفاعلات الأكسدة انتقال الإلكترونات من ذرة إلى أخرى. والاختزال . وكيف يتغير كل منهما في التفاعل؟ عندما تختزل ذرة أو أيون يقل عدد 11. اكتب معادلة تفاعل فلز الحديد مع حمض الهيدروبروميك لتكوين بروميد الحديد III وغاز الهيدروجين. ثم حدّد التغير الكلي في عدد تأكسد العنصر تأكسدها، وعندما تتأكسد ذرة أو أيون يزداد عدد تأكسدها. في تفاعلات الأكسدة والاختزال التي الذي اختزل والعنصر الذي تأكسد. 12. حدّد عدد التأكسد للعنصر الذي يظهر باللون الداكن في المركبات الآتية: Ca3N2 b HNO3 .a CuWO4 .d Sb2O5 .c تتضمن مركبات جزيئيةً وأيونات متعددة : 13. حدد عدد التأكسد للعنصر الذي يظهر باللون الداكن في الأيونات الآتية: MnO4 .b IO4 .a NH2 .d B4O72- .c الذرات بروابط تساهمية، فالذرات الأعلى كهروسالبية تختزل، في حين تتأكسد : 14. الرسم البياني واستعماله تعدُّ الفلزات القلوية عوامل مختزلة قوية. ارسم رسما بيانيًا توضح فيه كيف تزداد أو تقل قابلية الفلزات القلوية للاختزال الذرات ذات الكهروسالبية الأقل. كلما اتجهنا أسفل المجموعة ابتداءً من الصوديوم حتى الفرانسيوم. وزارة التعليم Ministry of Education 2024-1446 112

خلاصة درس الأكسدة والاختزال
تعد الفلزات القلوية عوامل مختزلة قوية ارسم رسما بيانيا توضح فيه كيف تزداد أو تقل قابلية الفلزات القلوية للاختزال



 2
2