تطور الجدول الدوري الحديث - الكيمياء2-1 - ثاني ثانوي
الفصل1: الحسابات الكيميائية
الفصل2: الإلكترونات في الذرات
الفصل3: الجدول الدوري والتدرج في خواص العناصر
الفصل4: المركبات الأيونية والفلزات
Ministry of Education 2024-1446 الجدول الدوري والتدرج في خواص العناصر The Periodic Table and Periodic Trends Oxygen 8 F 14.007 15.999 18.998 Phosphory 15 Chlorine 17 Sulfur P CI 16 30.97 35.453 S Arsen 32.066 33 3 34 Bromine 35 A Se Br 78.96 79 Phosph الأكسجين الكبريت Carbon 6 NIL 7 B 10.811 N 12.011 14.007 Aluminum 13 Phosphorus 15 Silicon Al P 14 26.98 30.974 Si Galliu 31 28.086 Arsenic 32 33 Ge As 72.64 7^ gen Fluorine 7 9 Oxygen N F 8 14.00 18.998 O 15.999 Chlorine 15 16 17 P S CI 30.974 32.066 35.453 rsenic Selenium Bromine 34 35 Se السليكون 3 الفصل الفكرة العامة ( يتيح لنا التدرج في خواص ذرات العناصر في الجدول الدوري التنبؤ بالخواص الفيزيائية والكيميائية لها . 3-1 تطور الجدول الدوري الحديث الفكرة الرئيسة لقد تطور الجدول الدوري تدريجيا مع الوقت باكتشاف العلماء طرائق أكثر فائدة في تصنيف العناصر ومقارنتها. 3-2 تصنيف العناصر الفكرة الرئيسة رتبت العناصر في الجدول الدوري ضمن مجموعات ودورات حسب أعدادها الذرية . 3- تدرج خواص العناصر الفكرة الرئيسة يعتمد تدرج خواص العناصر في الجدول الدوري على حجوم الذرات وقابليتها لفقدان الإلكترونات واكتسابها. حقائق كيميائية يتضمن الجدول الدوري حاليا 118 عنصرًا، يوجد منها في الطبيعة 92 عنصرًا فقط. يُعد عنصر الهيدروجين أكثر العناصر توافرًا في الكون ونسبة كتلته %75 ، في حين يُعد عنصر الأكسجين أكثر العناصر توافرًا في الأرض ونسبته %50. • يحتوي جسم شخص كتلته 70kg على والي 43kg تقريبًا من الأكسجين. تقل الكمية الكلية لعنصر الأستاتين في القشرة الأرضية عن g 30، مما يجعله أقل العناصر وفرة في الأرض. 104

يتضمن الجدول الدوري حاليا 118 عنصرا ويوجد منها في الطبيعة 92 عنصرا فقط
الجدول الدوري والتدرج في خواص العناصر
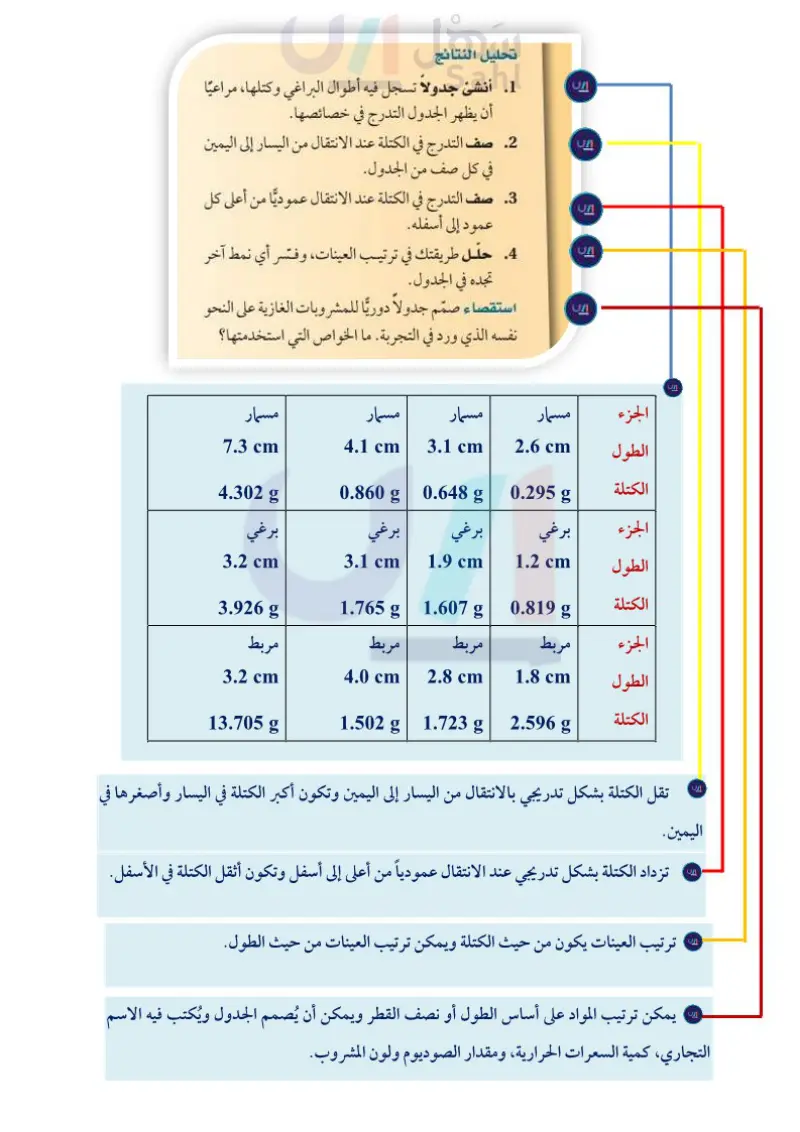
نشاطات تمهيدية تجربة استهلالية كيف تتمكن من تعرف أنماط التغير في الخواص؟ تترتب العناصر في الجدول الدوري بطريقة تسمح بتكرار خواصها على نحو منتظم. ويمكن تطبيق عملية تكرار الخواص على أشياء من البيئة. خطوات العمل B 1. اقرأ نموذج السلامة في المختبر. 2. أحضر عددًا من البراغي من ثلاثة أنواع مختلفة. .3 قس طول كل برغي بالمسطرة. .4 قس كتلة كل برغي بالميزان. رتب العينات تصاعديًا من حيث الطول والكتلة وفق شكلها. تحليل النتائج 1 أنشئ جدولاً تسجل فيه أطوال البراغي وكتلها، مراعيًا أن يظهر الجدول التدرج في خصائصها. 2 صف التدرج في الكتلة عند الانتقال من اليسار إلى اليمين في كل صف من الجدول. 3. صف التدرج في الكتلة عند الانتقال عموديًا من أعلى كل عمود إلى أسفله. 4. حلّل طريقتك في ترتيب العينات، وفسّر أي نمط آخر تجده في الجدول. استقصاء صمّم جدولاً دوريا للمشروبات الغازية على النحو نفسه الذي ورد في التجربة ما الخواص التي استخدمتها؟ المطويات منظمات الأفكار مطوية تساعدك على تنظيم المعلومات عن تدرج تدرج الخواص اعمل الخواص. خطوة 1 اطو قطعة الورق إلى 3 أقسام عرضيا. خطوة 2 اعمل طية بعرض 2cm على طول أحد الحواف، ثم اطو قطعة الورق من المنتصف عند هذا الخط، وكرر ذلك مرة أخرى. خطوة 3 افتح الورقة وارسم خطوطا على طول الطيات، وسمّم الأجزاء على النحو الآتي: تدرج لخواص، الدورات تدرج الخواص نصف قطر الذرة الدورات المجموعات الأيون نصف قطر طاقة التاين مقدار الكهرسالبية المجموعات نصف قطر الذرة نصف قطر الأيون، طاقة التأين، مقدار الكهروسالبية. المطويات استخدم هذه المطوية في القسم 3 -3، ولخص التدرج في خواص العناصر عبر الدورات والمجموعات. 105 واقيت عليم Ministry of Education 2024-1446

تدرج الخواص
3-1 رابط الدرس الرقمي الأهداف تطور الجدول الدوري الحديث www.ien.edu.sa تتبع مراحل تطور الجدول الدوري Development of the Modern Periodic Table تعرف الملامح الرئيسة في الجدول الدوري. مراجعة المفردات الفكرة الرئيسة لقد تطوّر الجدول الدوري للعناصر تدريجيًا مع الوقت باكتشاف العلماء طرائق أكثر فائدة في تصنيف العناصر ومقارنتها. الربط مع الحياة كيف تبدو عملية التسوق إذا أردت شراء بعض الفاكهة وقد اختلط التفاح العدد الذري : عدد البروتونات في بالكمثرى بالبرتقال بالخوخ في سلة واحدة؟! لذا، من هنا تتضح أهمية تصنيف الأشياء حسب خواصها. لذا يصنف العلماء العناصر المختلفة حسب خواصها في الجدول الدوري. الذرة. المفردات الجديدة التدرج في الخواص المجموعات الدورات العناصر الممثلة العناصر الانتقالية الفلزات الفلزات القلوية الفلزات القلوية الأرضية الفلزات الانتقالية الفلزات الانتقالية الداخلية سلسلة اللانثانيدات سلسلة الأكتنيدات اللافلزات الهالوجينات تطور الجدول الدوري Development of the Periodic Table قام العالم الفرنسي أنتوني لا فوازييه Lavoisier في أواخر القرن الثامن عشر (17941743م) بتجميع العناصر المختلفة المعروفة آنذاك في قائمة واحدة وتحتوي هذه القائمة المتضمنة في الجدول 31 على 33 عنصرًا موزعة على 4 فئات. جون نيولاندز John Newlands اقترح الكيميائي الإنجليزي جون نيولاندز عام 1864م مخططًا تنظيميا للعناصر ؛ فقد لاحظ أن الخواص تتكرر عند ترتيبها تصاعديا وفق تسلسل الكتل الذرية لكل ثمانية عناصر . ويسمى هذا النمط بالدورية؛ لأنه يتكرر بالنمط نفسه. ولقد قام نيو لاندز بتسمية هذه العلاقة الدورية بقانون الثمانيات. ويوضح الشكل 1-3 طريقة نيولاندز في ترتيب 14 عنصرًا كانت معروفة في أواسط عام 1860م. وقد واجه قانون الثمانيات معارضة؛ لأنه لا يمكن تطبيقه على العناصر المعروفة جميعها آنذاك. كما أن العلماء لم يتقبلوا كلمة الثمانيات. وعلى الرغم من أن القانون لم يحظ بموافقة الجميع، إلا أنه مع مرور بعض السنوات بدا جليا أن نيولاندز كان على صواب؛ إذ تتكرر خواص العناصر بشكل دوري كل ثمانية عناصر . الغازات النبيلة أشباه الفلزات الجدول 1-3 الغازات جدول لافوازييه للمواد البسيطة الضوء، الحرارة، الأكسجين، النيتروجين، الهيدروجين. الفلزات الأنتمون الفضة الزرنيخ البزموث، الكوبلت النحاس، القصدير، الحديد، المنجنيز، الزئبق، الموليبديوم، النيكل، الذهب، البلاتينيوم، الرصاص، التنجستون، الخارصين (الزنك). اللافلزات الكبريت، الفوسفور، الكربون، حمض الهيدروكلوريك، حمض الهيدروفلوريك، حمض البوريك. 106 العناصر الأرضية الطباشير، الماغنسيا (أكسيد الماغنسيوم)، البورات الصلصال، السليكا (أكسيد السليكون). وزارة التعليم Ministry of Education 2024-1446

ماير ومندليف Meyer and Mendeleev في عام 1869م قام كل من الكيميائي العناصر ذات الخواص المتشابهة تقع في الصف نفسه الألماني لوثر ماير (1830 - 1895م) والكيميائي الروسي ديمتري مندليف (1834- 1907م) بتقديم الدليل على العلاقة بين العدد الكتلي للعناصر وخواصها. وقد حظي مندليف بسمعة أكثر من ماير؛ حيث قام بنشر دراسته أولاً. لاحظ مندليف – كما لاحظ نیولاندز قبل عدة سنوات - أنه عند ترتيب العناصر تصاعديا وفق كتلها الذرية فإن خواصها تتكرر وفق نمط ،دوري، فقام بتشكيل الجدول الدوري بترتيب العناصر تصاعديا وفق كتلها الذرية في أعمدة تحوي العناصر المتشابهة في خواصها. ... إلخ A H 1 A F 8- B Li 2 B Na 9 C G 3 C Mg 10 D BO 4 D Al 11 EC 5 E Si 12 FN 6 FP 13 GO7 GS 14 مجموعة واحدة وقد لاقى جدول مندليف - كما في الشكل 2-3 - قبولا واسعا؛ حيث أمكنه توقع وجود عناصر لم تكتشف بعد وحدّد خواصها، كما ترك مندليف أماكن شاغرة في الجدول للعناصر التي اعتقد أنها لم تكتشف بعد. وقد تمكّن مندليف من خلال ملاحظة أنماط الشكل 1-3 لاحظ جون نيولاندز أن التغير في خواص العناصر المعروفة من توقع خواص العناصر التي سيتم اكتشافها، ومنها خواص العناصر تتكرر كل 8 عناصر. السكانديوم، والجاليوم، والجيرمانيوم. موزلي Mosley لم يكن جدول مندليف صحيحًا تمامًا؛ فبعد اكتشاف العديد من العناصر الجديدة، وتحديد الكتل الذرية للعناصر المعروفة بدقة أكثر، بدا واضحًا أن بعض العناصر لم توضع في مكانها الصحيح في الجدول. إذ إن ترتيب العناصر وفق كتلها الذرية أدى إلى وضع بعض العناصر في مجموعات لعناصر ذات خواص مختلفة عنها . فقام الكيميائي الإنجليزي هنري موزلي (1887 - 1915م) في عام 1913م بتحديد سبب . هذه المشكلة؛ إذ اكتشف أن ذرات كل عنصر تحتوي على عدد محدد وفريد من البروتونات في أنويتها - وبناءً على ذلك رتبت العناصر في الجدول الدوري تصاعديا وفق أعدادها الذرية. وقد نتج عن ترتيب موزلي للعناصر وفق عددها الذري أنماط أكثر وضوحًا في تدرج خواصها. ويُعرف تكرار الخواص الكيميائية والفيزيائية عند ترتيب العناصر تصاعديا وفق أعدادها الذرية بتدرج الخواص. ماذا قرأت ؟ قارن بين طريقة كل من مندليف وموزلي في ترتيب العناصر. الشكل 2-3 قام مندليف في النسخة الأولى للجدول الذي نشره في عام 1869م بترتيب العناصر ذات الخواص الكيميائية المتشابهة أفقيًا. وقد ترك أماكن فارغة للعناصر التي لم تكن قد اكتشفت في 107 واقيت عليم Ministry of Education 2024-1446 ذلك الوقت. K = 39 Ca = 40 =55 335 Rb = 85 Sr = 87 ? Yt Ti=48? Zr = 90 Nb = 94 V = 51 Mo = 96 Cr=52 Mn Cs = 133 Ba=137 88?? Di=138? Er 178? = Ce 140??La=180? Th=281 Ta= 182 W = 184 - U = 240 - 56 Fe= Co=59 Ni=59 - Ru=104 Rh=104 Pd=106 Ag <=108 Cd=112 In = 113 Sn=118 Sb=122 Te = 125? <=127 J - Os=195? Ir = 197 Pt=198? Au == 199? <=200 Hg: T1 = 204 Pb=207 Bi=208 - Typische Elemente H=1 Li= 7 Na == 23 Be = 9,4 Mg <<=24 Cu = 63 Zn=65 B = 11 Al ======= 27,3 - C =12 Si ==28 N = 14 P <=31 = 16 S =32 As ==== 75 So=78 F <=19 Cl Br=80 = 35,5

المفردات أصل الكلمة الدورية Periodic جاءت الكلمة periodos من أصل لاتيني وتعني الطريق الدائري. يلخص الجدول 2-3 مساهمات كل من نيولاندز وماير ومندليف وموزلي في تطوير الجدول الدوري. وأصبح هذا الجدول من أهم الأدوات التي يستخدمها الكيميائيون. ويعد الجدول الدوري مرجعًا مهما لفهم خواص العناصر، والتنبؤ بها وتنظيم المعلومات المتعلقة بالتركيب الذري. الجدول 2-3 جون نیولاندز 1837-1898م المساهمات في تصنيف العناصر • رتب العناصر تصاعديا وفق الكتل الذرية. . لاحظ تكرار خواص العناصر لكل ثمانية عناصر . • وضع قانون الثمانيات. لوثر ماير 1830-1895م . أثبت وجود علاقة بين الكتل الذرية وخواص العناصر . • رتب العناصر تصاعديا وفق الكتل الذرية. ديمتري مندليف 1834-1907م . أثبت وجود علاقة بين الكتل الذرية وخواص العناصر. • رتب العناصر تصاعديا وفق الكتل الذرية. • تنبأ بوجود عناصر غير مكتشفة، وحدد خواصها. هنري موزلي 1887-1915م ، اكتشف أن العناصر تحتوي على عدد فريد من البروتونات سماه العدد الذري. . رتب العناصر تصاعديا وفق العدد الذري، مما نتج عنه نموذج لدورية خواص العناصر. الجدول الدوري الحديث اسم العنصر الحالة الكتلة الذرية المتوسطة أكسجين 8 O 15.999 العدد الذري الرمز الشكل 3- تحتوي المربعات في الجدول الدوري على اسم العنصر والرمز الكيميائي والعدد الذري والكتلة الذرية وحالة المادة. The Modern Periodic Table يتكون الجدول الدوري الحديث من مجموعة مربعات يحتوي كل مربع على اسم العنصر ورمزه وعدده الذري وكتلته الذرية . ويوضح الشكل 3-3 أحد هذه المربعات. وقد رتبت المربعات تصاعديا وفق العدد الذري في سلسلة من الأعمدة الرأسية تُعرف بالمجموعات أو العائلات، وفي صفوف أفقية تُعرف بالدورات. ويوضح الشكل 5- الجدول الدوري للعناصر . ماذا قرأت ؟ عرّف المجموعات والدورات. 108 وزارة التعليم Ministry of Education 2024-1446

الدورية
يحتوي الجدول الدوري الحديث على سبع دورات بدءًا من الهيدروجين في الدورة الأولى. وقد رقمت المجموعات من 1 إلى 18 فمثلا تحتوي الدورة الرابعة على البوتاسيوم والكالسيوم، في حين يوجد السكانديوم Sc في العمود الثالث من اليسار، أي في المجموعة الثالثة. ويوجد الأكسجين في المجموعة 16 وكما أن لعناصر المجموعات 1 و 2 و 13 - 18 الكثير جدا من الخواص الفيزيائية والكيميائية، لذلك يشار إليها بعناصر المجموعات الرئيسة أو العناصر الممثلة. ويُشار إلى عناصر المجموعات من 3 إلى 12 بالعناصر الانتقالية. كما تُصنّف العناصر إلى فلزات ولافلزات وأشباه فلزات. الفلزات تُسمى العناصر التي تكون ملساء ولامعة وصلبة في درجة حرارة الغرفة وجيدة التوصيل للحرارة والكهرباء بالفلزات. ويمتاز معظمها بأنه قابل للطرق والسحب؛ إذ يمكن تحويلها إلى صفائح رقيقة، وسحبها إلى أسلاك رفيعة. ومعظم العناصر الممثلة والعناصر الانتقالية فلزات وإذا نظرت إلى عنصر البورون B في العمود 13، تشاهد خطا متعرجًا يصل إلى الأستاتين At في أسفل المجموعة 17. ويفصل هذا الخط بين الفلزات واللافلزات في الجدول الدوري. وقد مثلت الفلزات بالمربعات ذات اللون الأزرق في الشكل 5-3. الفلزات القلوية العناصر عن يسار الجدول جميعها فلزات إلا الهيدروجين، وتُسمى عناصر المجموعة 1 (ما عدا الهيدروجين) الفلزات القلوية . ونظرًا إلى شدة نشاطها فهي غالبًا ما تكون موجودة في الطبيعة على هيئة مركبات مع عناصر أخرى. ومن الفلزات القلوية الشائعة الصوديوم Na وهو أحد مكونات ملح الطعام، والليثيوم Li المستخدم في البطاريات. الفلزات القلوية الأرضية توجد الفلزات القلوية الأرضية في المجموعة 2، وهي أيضًا سريعة التفاعل. ويُعد عنصرا الكالسيوم Car والماغنسيوم Mg من الفلزات المفيدة لصحة الجسم، وهما من الفلزات القلوية الأرضية. والماغنسيوم صلب، ووزنه خفيف نسبيًّا، لذا يستخدم في تصنيع الأجهزة الإلكترونية، ومنها الحواسيب المحمولة، كما في الشكل 4-3 . الشكل 4-3 لأن الماغنسيوم خفيف وقوي يستخدم في تصنيع الأجهزة الإلكترونية. فمثلا الإطار الخارجي لهذا الحاسب الآلي المحمول مصنوع من الماغنسيوم. 109 واقيت عليم Ministry of Education 2024-1446

لأن الماغنسيوم خفيف وقوي يستخدم في تصنيع الأجهزة الإلكترونية
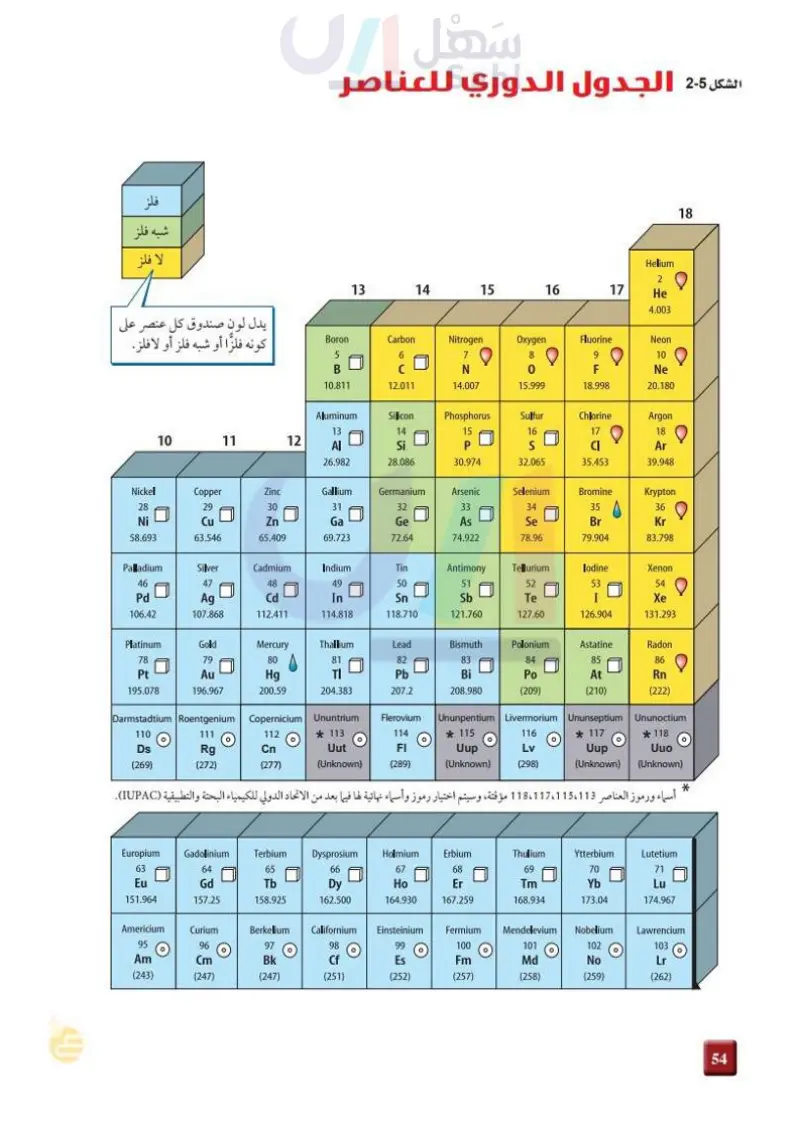
وزارة التعليم Ministry of Education 2024-1446 فلز شبه فلز لا فلز يدل لون صندوق كل عنصر على كونه فلزا أو شبه فلز أو لا فلز. الشكل 5-3 الجدول الدوري للعناصر Helium 2 13 14 15 16 17 He 4.003 Boron Carbon Nitrogen Oxygen Fluorine Neon 5 6 7 8 9 10 B C N 0 F Ne 10.811 12.011 14.007 15.999 18.998 20.180 Aluminum Silicon Phosphorus Sulfur Chlorine Argon 13 14 15 16 17 18 10 11 12 ΑΙ Si P S CI Ar 26.982 28.086 30.974 32.065 35.453 39.948 Nickel Copper Zinc Gallium Germanium Arsenic Selenium Bromine Krypton 28 29 30 31 32 33 34 35 36 Ni Cu Zn Ga Ge As Se Br Kr 58.693 63.546 65.409 69.723 72.64 74.922 78.96 79.904 83.798 Palladium Silver Cadmium Indium Tin Antimony Tellurium lodine Xenon 46 47 48 49 50 51 52 53 54 Pd Ag Cd In Sn Sb Te I Xe 106.42 107.868 112.411 114.818 118.710 121.760 127.60 126.904 131.293 Platinum Gold Mercury Thallium Lead Bismuth Polonium Astatine Radon 78 79 80 81 82 83 84 85 86 Pt Au Hg TI Pb Bi Po At Rn 195.078 196.967 200.59 204.383 207.2 208.980 (209) (210) (222) Darmstadtium Roentgenium Copernicium 110 111 112 Nihonium 113 Flerovium Moscovium Livermorium Tennessine Oganesson 114 115 116 117 118 ○ Ds (269) Rg Cn Nh FI Mc Lv Ts Og (272) 285.177 286.183 289.191 290.196 293.205 294.211 294.214 Europium Gadolinium Terbium Dysprosium Holmium Erbium Thulium Ytterbium Lutetium 63 64 65 66 67 68 69 70 71 Eu Gd Tb Dy Ho Er Tm Yb Lu 151.964 157.25 158.925 162.500 164.930 167.259 168.934 173.04 174.967 18 Americium Curium Berkelium Californium 95 96 97 98 Einsteinium 99 Fermium Mendelevium Nobelium Lawrencium 100 101 102 103 ○ ○ ○ ○ о Am Cm Bk Cf Es Fm Md No (243) (247) (247) (251) (252) (257) (258) (259) Lr (262) ○ 110

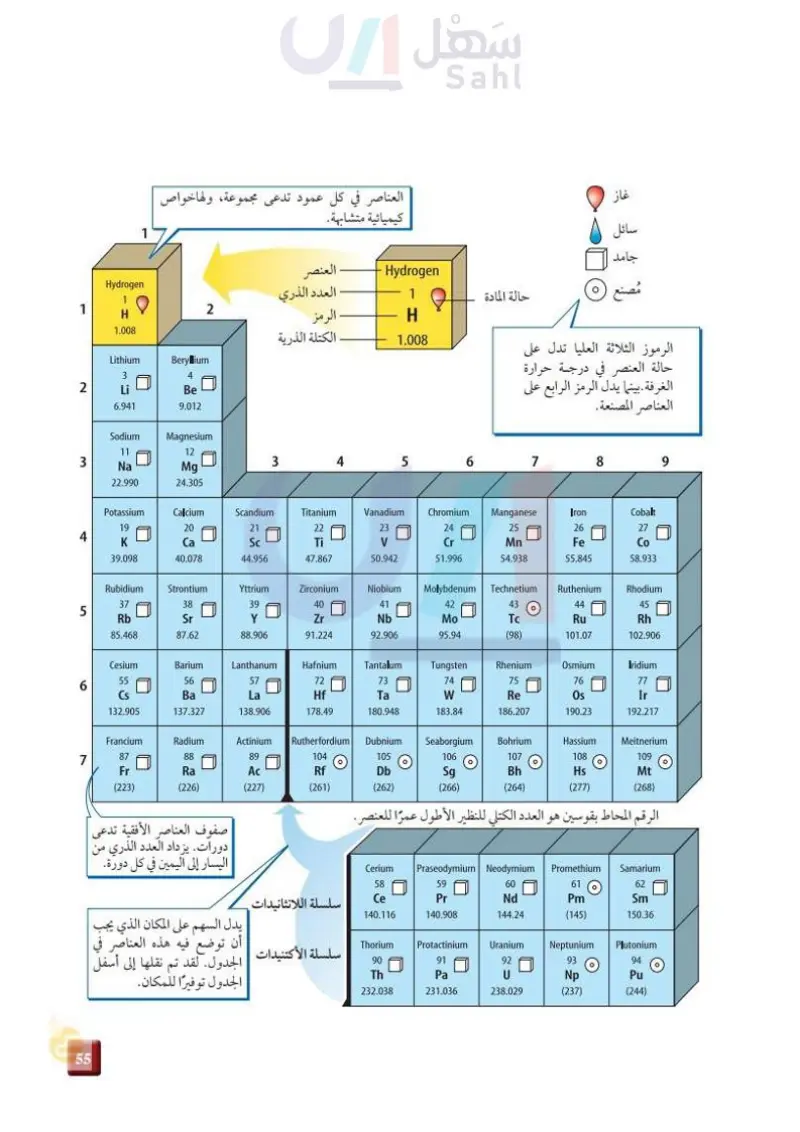
Hydrogen 1 العناصر في كل عمود تدعى مجموعة، ولهاخواص كيميائية متشابهة . 1 1 2 H 1.008 Lithium Beryllium 3 4 2 Li Be 6.941 9.012 العنصر العدد الذري الرمز الكتلة الذرية Hydrogen 1 H 1.008 غاز سائل جامد مصنع و حالة المادة الرموز الثلاثة العليا تدل على حالة العنصر في درجة حرارة الغرفة . بينما يدل الرمز الرابع على العناصر المصنعة. Sodium Magnesium 11 12 3 3 4 5 6 7 8 9 Na Mg 22.990 24.305 Potassium Calcium Scandium Titanium Vanadium Chromium Manganese Iron Cobalt 19 20 21 22 23 24 25 26 27 4 K Ca Sc Ti V Cr Mn Fe Co 39.098 40.078 44.956 47.867 50.942 51.996 54.938 55.845 58.933 Rubidium Strontium Yttrium Zirconium Niobium Molybdenum Technetium Ruthenium Rhodium 37 38 39 40 41 42 43 44 45 ○ 5 Rb Sr Y Zr Nb Mo Tc Ru Rh 85.468 87.62 88.906 91.224 92.906 95.94 (98) 101.07 102.906 Cesium Barium Lanthanum Hafnium Tantalum Tungsten Rhenium Osmium Iridium 55 56 57 72 73 74 75 76 77 6 Cs Ba La Hf Ta W Re Os Ir 132.905 137.327 138.906 178.49 180.948 183.84 186.207 190.23 192.217 Francium Radium Actinium Rutherfordium Dubnium Seaborgium Bohrium Hassium Meitnerium 7 87 88 89 104 105 106 107 108 109 ○ ○ O Fr Ra Ac Rf Db (223) (226) (227) (261) (262) Sg (266) Bh Hs Mt (264) (277) (268) 111 صفوف العناصر الأفقية تدعى دورات. يزداد العدد الذري من اليسار إلى اليمين في كل دورة. سلسلة اللانثانيدات سلسلة الأكتنيدات يدل السهم على المكان الذي يجب أن توضع فيه هذه العناصر في تم نقلها إلى أسفل الجدول. لقد الجدول توفيرا للمكان. Ministry of Education 2024-1446 الرقم المحاط بقوسين هو العدد الكتلي للنظير الأطول عمرًا للعنصر. Cerium Praseodymium Neodymium Promethium Samarium 58 59 60 61 62 Ce Pr Nd Pm Sm 140.116 140.908 144.24 (145) 150.36 Thorium Protactinium Uranium Neptunium Plutonium 90 91 92 93 94 Th Pa U Np Pu 232.038 231.036 238.029 (237) (244)

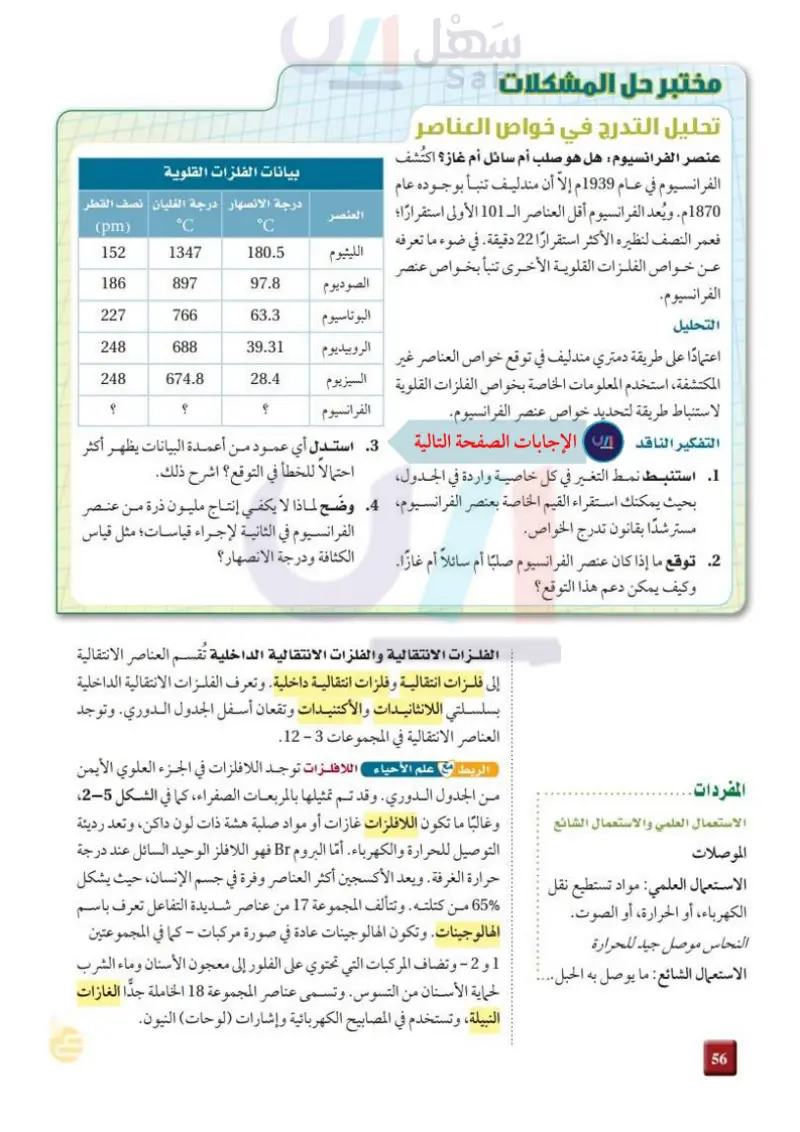
مختبر حل المشكلات تحليل التدرج في خواص العناصر عنصر الفرانسيوم: هل هو صلب أم سائل أم غاز؟ اكتشف الفرانسيوم في عام 1939م إلاّ أن مندليف تنبأ بوجوده عام 1870م. ويُعد الفرانسيوم أقل العناصر الـ 101 الأولى استقرارًا؛ فعمر النصف لنظيره الأكثر استقرارًا 22 دقيقة. في ضوء ما تعرفه عن خواص الفلزات القلوية الأخرى تنبأ بخواص عنصر العنصر الليثيوم الفرانسيوم. التحليل اعتمادًا على طريقة دمتري مندليف في توقع خواص العناصر غير المكتشفة، استخدم المعلومات الخاصة بخواص الفلزات القلوية لاستنباط طريقة لتحديد خواص عنصر الفرانسيوم. التفكير الناقد الصوديوم البوتاسيوم الروبيديوم السيزيوم الفرانسيوم بيانات الفلزات القلوية درجة الانصهار | درجة الغليان | نصف القطر (pm) °C 152 1347 180.5 186 897 97.8 227 766 63.3 248 688 39.31 248 674.8 28.4 ؟ 3. استدل أي عمود من أعمدة البيانات يظهر أكثر 1. استنبط نمط التغير في كل خاصية واردة في الجدول، احتمالاً للخطأ في التوقع؟ اشرح ذلك. بحيث يمكنك استقراء القيم الخاصة بعنصر الفرانسيوم .4 وضح لماذا لا يكفي إنتاج مليون ذرة من عنصر الفرانسيوم في الثانية لإجراء قياسات؛ مثل قياس مستر شدًا بقانون تدرج الخواص. 2 توقع ما إذا كان عنصر الفرانسيوم صلبًا أم سائلاً أم غازا. الكثافة ودرجة الانصهار؟ وكيف يمكن دعم هذا التوقع؟ المفردات الفلزات الانتقالية والفلزات الانتقالية الداخلية تُقسم العناصر الانتقالية إلى فلزات انتقالية وفلزات انتقالية داخلية. وتعرف الفلزات الانتقالية الداخلية بسلسلتي اللانثانيدات والأكتنيدات وتقعان أسفل الجدول الدوري. وتوجد العناصر الانتقالية في المجموعات 3 - 12. الربط مع علم الأحياء اللافلزات توجد اللافلزات في الجزء العلوي الأيمن من الجدول الدوري. وقد تم تمثيلها بالمربعات الصفراء، كما في الشكل 5-3، الاستعمال العلمي والاستعمال الشائع وغالبًا ما تكون اللافلزات غازات أو مواد صلبة هشة ذات لون داكن، وتعد رديئة الموصلات الاستعمال العلمي: مواد تستطيع نقل الكهرباء، أو الحرارة، أو الصوت. النحاس موصل جيد للحرارة الاستعمال الشائع : ما يوصل به الحبل. 65% التوصيل للحرارة والكهرباء. أما البروم Br فهو اللافلز الوحيد السائل عند درجة حرارة الغرفة. ويعد الأكسجين أكثر العناصر وفرة في جسم الإنسان، حيث يشكل من كتلته. وتتألف المجموعة 17 من عناصر شديدة التفاعل تعرف باسم الهالوجينات. وتكون الهالوجينات عادة في صورة مركبات – كما في المجموعتين 1 و 2 - وتضاف المركبات التي تحتوي على الفلور إلى معجون الأسنان وماء الشرب لحماية الأسنان من التسوس. وتسمى عناصر المجموعة 18 الخاملة جدا الغازات النبيلة، وتستخدم في المصابيح الكهربائية وإشارات (لوحات) النيون. 112 وزارة التعليم Ministry of Education 2024-1446

الموصلات
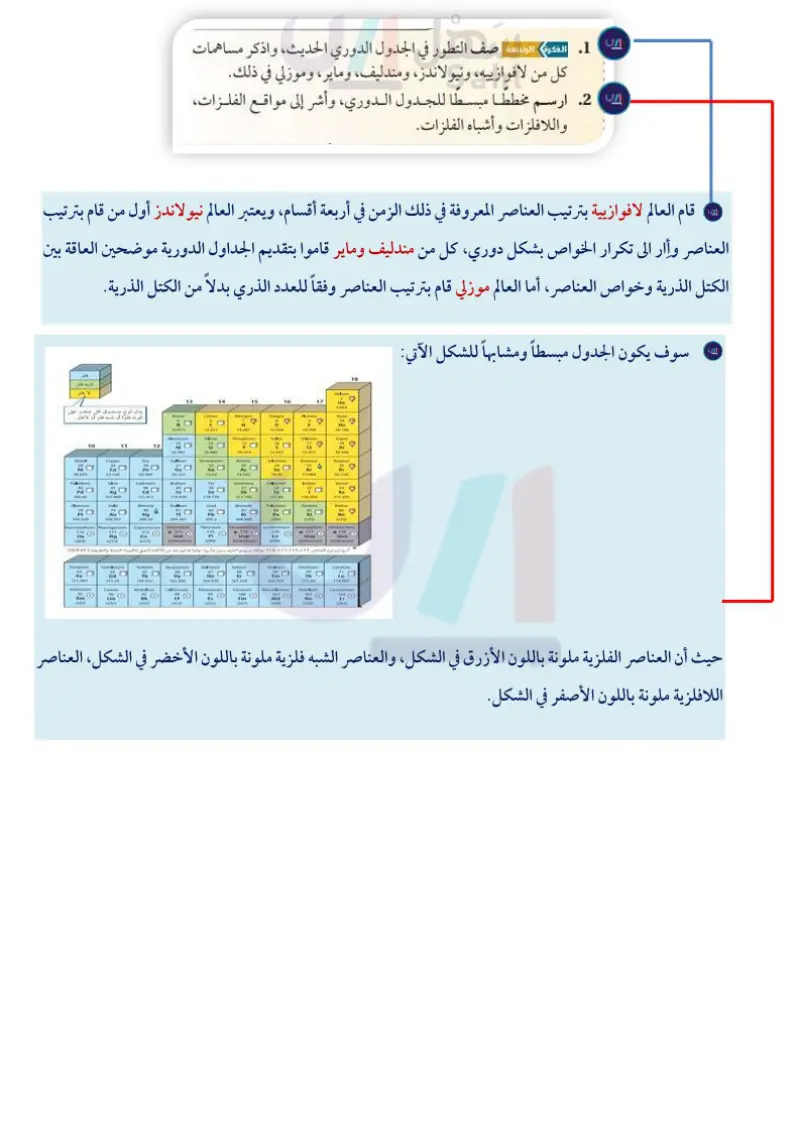
أشباه الفلزات تُعرف العناصر في المربعات الخضراء على جانبي الخط المتعرج في الشكل 5-3 بأشباه الفلزات. ولأشباه الفلزات خواص فيزيائية وكيميائية مشابهة للفلزات واللافلزات معا. فالسليكون Si والجرمانيوم Ge من أشباه الفلزات المهمة المستخدمة بكثرة في صناعة رقائق الحاسوب والخلايا الشمسية، كما يستخدم السليكون في الجراحة التجميلية والتطبيقات التي تحاكي الواقع، كما في الشكل 6-3. ويمكنك الرجوع إلى دليل العناصر الكيميائية في نهاية هذا الكتاب لمعرفة المزيد عن مجموعات العناصر. مختلف التقويم 1-3 الشكل 6-3 قام العلماء المهتمون بتطوير تقنيات الغواصات بصنع غواصة آلية على صورة سمكة، قادرة مثلها على السباحة. وصنع جسم الغواصة الآلية من راتنج السليكون الذي يصبح لينا في الماء. الخلاصة 1. الفكرة الرئيسة صف التطور في الجدول الدوري الحديث، واذكر مساهمات تم ترتيب العناصر قديماً في الجدول كل من لافوازييه ونيولاندز، ومندليف، وماير، وموزلي في ذلك. الدوري وفق كتلها الذرية تصاعدياً 2 ارسم مخططًا مبسطا للجدول الدوري، وأشر إلى مواقع الفلزات، واللافلزات وأشباه الفلزات. مما نجم عنه وضع بعض العناصر في غير أماكنها وقد تم ترتيبها لاحقاً وفقاً 3. صف الخواص العامة للفلزات واللافلزات وأشباه الفلزات. لتزايد أعدادها الذرية. تتدرج الخواص الفيزيائية والكيميائية للعناصر عند ترتيبها تصاعديا أعدادها الذرية. 4 حدّد أي العناصر الآتية عناصر ممثلة، وأيها عناصر انتقالية؟ a ليثيوم Li b. بلاتين Pt c.بروميثيوم Pm d.كربون C 5 قارن اكتب اسمي عنصرين لهما خصائص مشابهة لكل من : a. اليود I b. الباريوم Ba c. الحديد Fe تترتب العناصر في الجدول الدوري : 6 قارن استنادًا إلى الجدول الدوري ،الحديث ما العنصران اللذان تكون في دورات (صفوف) ومجموعات قيمة الكتلة الذرية لكل منهما أقل من ضعف عدده الذري؟ (أعمدة)، وتقع العناصر المتشابهة في 7. تفسير البيانات تخطط شركة لتصنيع جهاز إلكتروني، مما يتطلب استخدام خواصها في المجموعة نفسها. عنصر له خواص كيميائية شبيهة بالسليكون Si والرصاص Pb، والكتلة تصنف العناصر إلى فلزات، ولافلزات الذرية له أكبر من كتلة الكبريت S، ولكنها أقل من كتلة الكادميوم Cd. استخدم الجدول الدوري لتحديد العنصر الذي يمكن أن تستخدمه الشركة. وأشباه فلزات. 113 Ministry of Education 2024-1446

صف التطور في الجدول في الجدول الدوري الحديث واذكر مساهمات كل من لا فوزيه ونيو لاندز ومندليف وماير وموزلي في ذلك


تخطط شركة لتصنيع جهاز إلكتروني مما يتطلب استخدام عنصر له خواص كيميائية شبيهة بالسليكون والرصاص والكتلة الذرية له أكبر من كتلة الكبريت؟





 0
0