المقصود بالحسابات الكيميائية - الكيمياء2-1 - ثاني ثانوي
الفصل1: الحسابات الكيميائية
الفصل2: الإلكترونات في الذرات
الفصل3: الجدول الدوري والتدرج في خواص العناصر
الفصل4: المركبات الأيونية والفلزات
رابط الدرس الرقمي www.ien.edu.sa 1-3 الأهداف ) تصف العلاقات من معادلة كيميائية موزونة. خلال المقصود بالحسابات الكيميائية تذكر النسب المولية في Defining Stoichiometry المعادلة الكيميائية الموزونة. الفكرة الرئيسة تحدد كميةً كل مادة متفاعلة عند بداية التفاعل الكيميائي كمية المادة مراجعة المفردات المواد المتفاعلة : المواد التي يبدأ بها التفاعل الكيميائي. المفردات الجديدة الحسابات الكيميائية النسبة المولية الناتجة. الربط مع الحياة لعلك شاهدت شمعة تحترق. عندما تحترق الشمعة تمامًا، أو تُطفأ بالنفخ عليها، يتوقف تفاعل الاحتراق في كلتا الحالتين. علاقة المول بالجسيمات Particles and Mole Relationship هل فوجئت باختفاء اللون الأرجواني لبر منجنات البوتاسيوم عندما أضفت كبريتيت الصوديوم الهيدروجيني في أثناء التجربة الاستهلالية؟ إذا استنتجت أن برمنجنات البوتاسيوم قد استهلكت وأن التفاعل قد توقف فهذا صحيح . تتوقف التفاعلات الكيميائية عندما تستهلك إحدى المواد المتفاعلة. وعندما يخطط الكيميائي لتفاعل بر منجنات البوتاسيوم وكبريتيت الصوديوم الهيدروجيني فإنه يتساءل كم جرامًا من برمنجنات البوتاسيوم نحتاج لتتفاعل تمامًا مع كتلة محددة من كبريتيت الصوديوم الهيدروجيني ؟ . وقد تتساءل عند تحليل تفاعل البناء الضوئي ما الكمية التي نحتاج إليها من الماء وثاني أكسيد الكربون لتكوين كتلة محددة من السكر ؟ . إن الحسابات الكيميائية هي الطريقة الصحيحة للإجابة عن هذه الأسئلة. الحسابات الكيميائية تُسمى دراسة العلاقات الكمية بين المواد المتفاعلة والمواد الناتجة في التفاعل الكيميائي الحسابات الكيميائية. وتعتمد الحسابات الكيميائية على قانون حفظ الكتلة الذي ينص على أن المادة لا تفنى ولا تستحدث في التفاعل الكيميائي إلا بقدرة الله تعالى. وتساوي كمية المواد الناتجة عند نهاية أي تفاعل كيميائي كمية المواد المستخدمة في بداية التفاعل. لذا فإن مجموع كتل المواد المتفاعلة يساوي مجموع كتل المواد الناتجة. لاحظ تفاعل مسحوق الحديد Fe مع الأكسجين ، الموضح في الشكل 18 فعلى الرغم من تكون مركب جديد هو أكسيد الحديد Fe2O III فإن كتلة هذا المركب الجديد لا تختلف عن كتلة مادتي التفاعل. الشكل 8-1- تحدد المعادلة الكيميائية الموزونة لتفاعل الحديد والأكسجين العلاقة بين كمية المواد المتفاعلة والناتجة. وزارة التعليم Ministry of Education 2024-1446 26 26

علاقة المول بالجسيمات
الحسابات الكيميائية
الأهداف لدرس المقصود بالحسابات الكيميائية
تحدد كمية كل مادة متفاعلة عند بداية التفاعل الكيميائي كمية المادة الناتجة
تحدد المعادلة الكيميائية الموزونة لتفاعل الحديد والأكسجين العلاقة بين كمية المواد المتفاعلة والناتجة
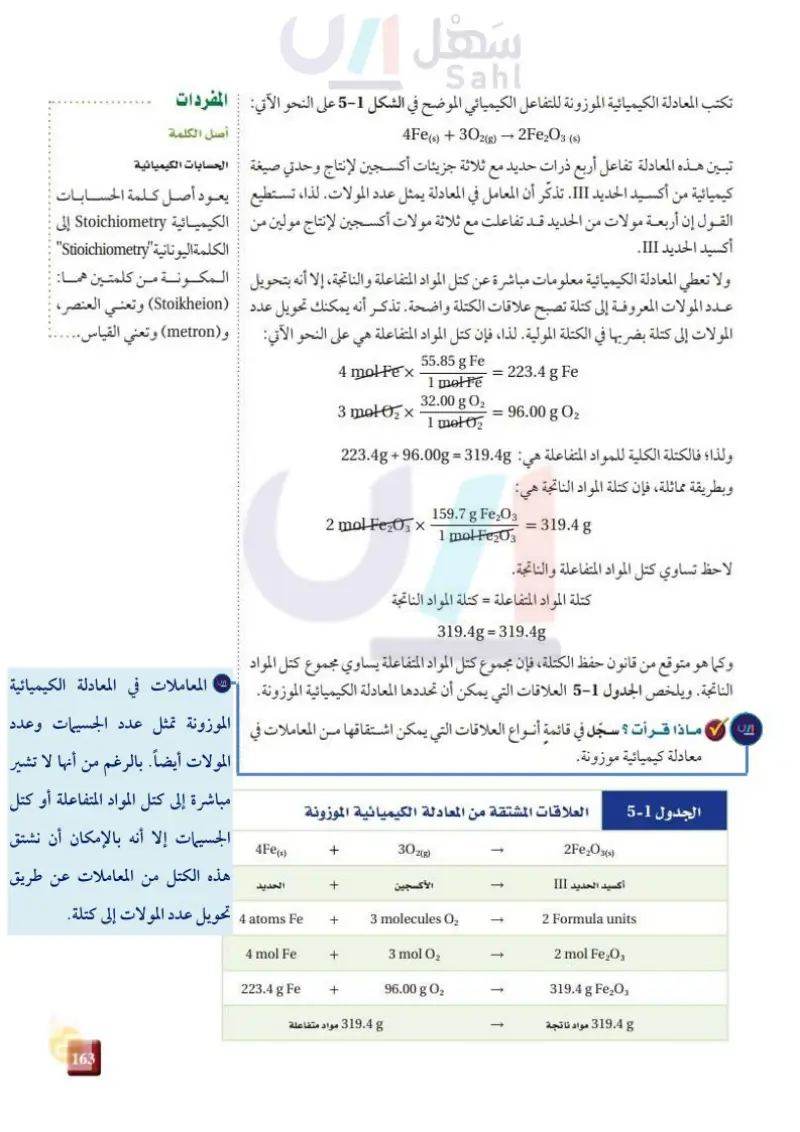
تكتب المعادلة الكيميائية الموزونة للتفاعل الكيميائي الموضح في الشكل 18 على النحو الآتي : المفردات 4Fe(s) + 302(g) → 2Fe2O3 (s) أصل الكلمة تبين هذه المعادلة تفاعل أربع ذرات حديد مع ثلاثة جزيئات أكسجين لإنتاج وحدتي صيغة الحسابات الكيميائية كيميائية من أكسيد الحديد .III تذكر أن المعامل في المعادلة يمثل عدد المولات. لذا، تستطيع يعود أصل كلمة الحسابات القول إن أربعة مولات من الحديد قد تفاعلت مع ثلاثة مولات أكسجين لإنتاج مولين من الكيميائية Stoichiometry إلى الكلمة اليونانية "Stioichiometry" أكسيد الحديد III. ولا تعطي المعادلة الكيميائية معلومات مباشرة عن كتل المواد المتفاعلة والناتجة ، إلا أنه بتحويل المكونة من كلمتين هما: عدد المولات المعروفة إلى كتلة تصبح علاقات الكتلة واضحة تذكر أنه يمكنك تحويل عدد (Stoikheion) وتعني العنصر، المولات إلى كتلة بضربها في الكتلة المولية. لذا، فإن كتل المواد المتفاعلة هي على النحو الآتي: و (metron) وتعني القياس 27 Ministry of Education 2024-1446 4 mol Fe x 55.85 g Fe = 223.4 g Fe 1 mol Fe 32.00 g O2 3 mol 02 x == 96.00 g O2 1 mol 02 ولذا؛ فالكتلة الكلية للمواد المتفاعلة هي : 319.48 = 223.4g + 96.00g وبطريقة مماثلة، فإن كتلة المواد الناتجة هي: 159.7 g Fe2O3 2 mol Fe2O3 × = 319.4 g 1 mol Fe2O3 لاحظ تساوي كتل المواد المتفاعلة والناتجة. كتلة المواد المتفاعلة = كتلة المواد الناتجة 319.4g = 319.4g وكما هو متوقع من قانون حفظ الكتلة، فإن مجموع كتل المواد المتفاعلة يساوي مجموع كتل المواد الناتجة. ويلخص الجدول -2- العلاقات التي يمكن أن تحددها المعادلة الكيميائية الموزونة. ماذا قرأت ؟ سجل في قائمة أنواع العلاقات التي يمكن اشتقاقها من المعاملات في معادلة كيميائية موزونة الجدول 2-1 العلاقات المشتقة من المعادلة الكيميائية الموزونة 4Fe(s) + 302(g) الحديد + الأكسجين 4 atoms Fe + 3 molecules O2 4 mol Fe + 3 mol 02 223.4 g Fe + 96.00 g O2 319.4 مواد متفاعلة ↑ ↑ ↑ T 2Fe2O3(s) III أكسيد الحديد 2 Formula units 2 mol Fe2O3 319.4 g Fe2O3 319.4 مواد ناتجة

سجل في قائمة أنواع العلاقات التي يمكن اشتقاقها من معادلة كيميائية موزونة
أصل الكلمة الحسابات الكيميائية
تكتب المعادلة الكيميائية الموزونة للتفاعل الكيميائي الموضح في الشكل 8-1 على النحو الآتي:
العلاقات المشتقة من المعادلة الكيميائية الموزونة
28 88 مثال 6-1 تفسير المعادلات الكيميائية يزودنا احتراق البروبان C بالطاقة اللازمة لتدفئة البيوت، وطهو الطعام، ولحام الأجسام الفلزية. فسر معادلة احتراق البروبان باستخدام عدد الجسيمات وعدد المولات والكتلة، ثم وضح تطبيق قانون حفظ الكتلة. 1 تحليل المسألة تمثل معاملات المعادلة الكيميائية الموضحة أدناه كلًا من المولات والجسيمات الممثلة في هذه الحالة الجزيئات). وسيتم إثبات قانون حفظ الكتلة إذا كانت كتل المواد المتفاعلة والمواد الناتجة متساوية. المعطيات C3H8(g)+5O2(g)→ 3CO2(g) +4H2O(g) 2 حساب المطلوب تحدد المعاملات في المعادلة الكيميائية عدد الجزيئات. المطلوب عدد الجزيئات = ؟ عدد المولات = ؟ كتل المواد المتفاعلة والناتجة = ؟ 1 molecule C3H8 + 5 molecules O2 → 3 molecules CO2 + 4 molecules H2O وتحدد المعاملات في المعادلة الكيميائية عدد المولات أيضًا. 1 mol C3H8 + 5 mol O2 → 3 mol CO2 + 4 mol H₂O وللتأكد من حفظ الكتلة نحول أولاً عدد مولات المواد المتفاعلة والمواد الناتجة إلى كتلة، وذلك بالضرب في معامل التحويل الكتلة المولية، التي تربط بين الجرامات والمولات. مولات المواد الناتجة أو المتفاعلة الكتلة المولية للمادة المتفاعلة أو الناتجة 1 مول مادة متفاعلة أو ناتجة جرامات المواد المتفاعلة أو المواد الناتجة. حساب كتلة و المتفاعلة. حساب كتلة 02 المتفاعلة. حساب كتلة CO2 الناتجة حساب كتلة H2O الناتجة اجمع كتل المواد المتفاعلة اجمع كتل المواد الناتجة تطبيق قانون حفظ الكتلة تقويم الإجابة 1 mol C H × 44.09 g C H Lmol CH === 44.09 g C H 5 mol O × = 160.0 g O 3mel CO x = 132.0 g CO 4 mol H Ox 72.08 g H 32.00 g O Lmoto 44.01 g CO Lmol CO 18.02 g H 1 mol H 44.09 g C H + 160.0 g O = 204.1 g 132.0 g CO + 72.08 g H O = 204.1 g مواد ناتجة g 204.1 = مواد متفاعلة g 204.1 إن مجموع كتل المواد المتفاعلة تساوي مجموع كتل المواد الناتجة، كما هو متوقع من قانون حفظ الكتلة. وزارة التعليم Ministry of Education 2024-1446

تفسير المعادلات الكيميائية يزودنا احتراق البروبان C3H8 بالطاقة اللازمة لتدفئة البيوت وطهو الطعام ولحام الأجسام الفلزية فسر معادلة احتراق البروبان باستخدام عدد الجسيمات وعدد المولات والكتلة ثم
مسائل تدريبية 30 فسر المعادلات الكيميائية الموزونة الآتية من حيث عدد الجسيمات والمولات والكتلة، آخذا بعين الاعتبار قانون حفظ الكتلة : N2(g) + 3H2(g) → 2NH 3(g) .a HCl(aq) + KOH (aq) → KCl(aq) + H2O() .b 2Mg(s) + O2(g) → 2MgO (s) 31. تحفيز زن المعادلات الكيميائية الآتية، ثم فسرها من حيث عدد الجسيمات الممثلة والمولات والكتلة الاعتبار قانون حفظ الكتلة : Zn(s) + _Na(s) + HNO3(aq) → _ Zn(NO3)2(aq) + _ N₂O(g) + H₂O(1) →> _NaOH(aq) + H2(g) .a H2O . (1) آخدًا بعين تجربة عملية تحديد نسب التفاعل نسبة المولات لقد تعلمت أن المعاملات في المعادلة الكيميائية تظهر العلاقات بين مولات المواد المتفاعلة ومولات المواد الناتجة. وتستطيع أن تستخدم العلاقات بين المعاملات لاشتقاق عوامل التحويل المسماة النسب المولية والنسبة المولية نسبة بين أعداد المولات ارجع إلى دليل التجارب العملية على منصة لأي مادتين في المعادلة الكيميائية الموزونة. فعلى سبيل المثال، يوضح تفاعل الشكل 9-1 تفاعل البوتاسيوم مع البروم B لتكوين بروميد البوتاسيوم KBr . ويستعمل الأطباء البيطريون الملح الأيوني الناتج عن التفاعل (بروميد البوتاسيوم) دواء مضادا للصرع عند الكلاب والقطط. 2 2K(s) +Br2(1) → 2KBr (s) فأي نسب مولية يمكن كتابتها لهذا التفاعل ؟ تستطيع بدءًا بالبوتاسيوم المتفاعل كتابة النسبة المولية التي تربط بين مولات البوتاسيوم وكل من المادتين الأخريين في المعادلة. ولذلك تربط إحدى النسب المولية بين مولات البوتاسيوم ومولات البروم المتفاعلة. في حين تربط النسبة الأخرى مولات البوتاسيوم المتفاعلة مع مولات بروميد البوتاسيوم الناتجة. 2 mol K 1 mol Brz و 2 mol K 2 mol KBr عين الإثرائية الشكل 9-1 يتفاعل فلز تظهر النسبتان الآتيتان كيف ترتبط مولات البروم مع مولات المادتين الأخريين في البوتاسيوم وسائل البروم المعادلة وهما: البوتاسيوم وبروميد البوتاسيوم. 1 mol Brz 2 mol K و 1 mol Bra 2 mol KBr وترتبط بصورة مماثلة نسبتا مولات بروميد البوتاسيوم مع مولات البوتاسيوم والبروم. 2 mol KBr 2 mol K و 2 mol KBr 1 mol Brz وتحدد هذه النسب الست علاقات المول في هذه المعادلة؛ إذ تشكل كل مادة من المواد الثلاث في المعادلة نسبة مع المادتين الأخريين. ماذا قرأت؟ حدد المصدر الذي تُشتق منه النسب المولية للتفاعل الكيميائي. بشدة لتكوين المركب الأيوني بروميد البوتاسيوم. 29 Ministry of Education 2024-1446

فسر المعادلات الكيميائية الموزونة الاتية من حيث عدد الجسيمات و المولات والكتلة، آخذا بعني الاعتبار قانون حفظ الكتلة:
حدد المصدر الذي تشتق منه النسب المولية للتفاعل الكيميائي
.زن المعادلات الكيميائية الآتية، ثم فسرها من حيث عدد الجسيمات الممثلة والمولات والكتلة آخذا بعين الاعتبار قانون حفظ الكتلة:
نسبة المولات
تحديد نسب التفاعل
يتفاعل فلز البوتاسيوم وسائل البروم بشدة لتكوين المركب الأيوني بروميد البوتاسيوم
مسائل تدريبية 32. حدد النسب المولية جميعها لكل من المعادلات الكيميائية الموزونة الآتية: 4Al(s) + 302(g) 2Al2O3(s) .a 3Fe(s) + 4H2O (1) → Fe3O4(s) + 4H2(g) .b 2HgO(s) →> 2Hg(1) + O2(g) .C .33. تحفيز زن المعادلات الآتية، ثم حدد النسب المولية الممكنة: ZnO (s) + HCl(aq) → ZnCl2(aq) + H2O(1) .a C4H10(g) + O2(g) → CO2(g) + H2O .b (g) لاحظ أن عدد النسب المولية التي يمكن كتابتها لتفاعل يحوي (n) من المواد هي (1-n(n. لذا، فالتفاعلات التي فيها 4، 5 مواد يمكن كتابة 12 و 20 نسبة مولية منها على التوالي. التفاعل الذي فيه 4 مواد: 12 = (1-4)4 التفاعل الذي فيه 5 مواد: 20 = (1-5) التقويم 3-1 الخلاصة و تُفسَّر المعادلة الكيميائية الموزونة على 34. الفكرة الرئيسة | قارن بين كتل المواد المتفاعلة والمواد الناتجة في التفاعل الكيميائي، ووضح العلاقة بين هذه الكتل. أساس المولات والكتلة والجسيمات 35. حدد عدد النسب المولية التي يمكن كتابتها لتفاعل كيميائي يوجد الممثلة (ذرات ، جزيئات، وحدات صيغ كيميائية). فيه ثلاث مواد. .36 صنف طرائق تفسير المعادلة الكيميائية الموزونة. يطبق قانون حفظ الكتلة على التفاعلات : 37. طبق المعادلة العامة لتفاعل كيميائي : الكيميائية جميعها. تشتق النسب المولية من معاملات المعادلة الكيميائية الموزونة. وترمز كل xA + yB → zAB حيث يمثل A و B عنصرين، وتمثل X و Y و المعاملات . حدد النسب المولية لهذا التفاعل. نسبة مولية إلى نسبة عدد مولات إحدى 38. طبق يتفكك فوق أكسيد الهيدروجين لينتج الماء والأكسجين. المواد المتفاعلة أو الناتجة، لعدد مولات اكتب معادلة كيميائية موزونة لهذا التفاعل، ثم حدد النسب المولية. مادة أخرى متفاعلة أو ناتجة في التفاعل 39. نمذج اكتب النسب المولية لتفاعل غاز الهيدروجين مع غاز الكيميائي. الأكسجين 2H2 + 02 →2H2O. مع العدد المناسب من ارسم 6 جزيئات هيدروجين تتفاعل جزيئات الأكسجين، ثم وضح عدد جزيئات الماء المتكوّنة. 30 وزارة التعليم Ministry of Education 2024-1446

حدد النسب المولية جميعها لكل من المعادلات الكيميائية الموزونة الاتية
خلاصة درس المقصود بالحسابات الكيميائية
قارن بين كتل المواد المتفاعلة والمواد الناتجة في التفاعل الكيميائي، ووضح العلاقة بين هذه الكتل.
صنف طرائق تفسير المعادلة الكيميائية الموزونة
طبق المعادلة العامة لتفاعل كيميائي:
زن المعادلات الآتية ثم حدد النسب المولية الممكنة:
لاحظ أن عدد النسب المولية التي يمكن كتابتها لتفاعل حيوي (n)من المواد هي (1-n)n
حدد عدد النسب المولية التي يمكن كتابتها لتفاعل كيميائي يوجد فيه ثالث مواد.
طبق يتفكك فوق أكسيد الهيدروجين لينتج الماء والأكسجين اكتب معادلة كيميائية موزونة لهذا التفاعل، ثم حدد النسب المولية.
ارســم 6 جزيئات هيدروجين تتفاعل مع العدد المناســب من جزيئات الأكسجين، ثم وضح عدد جزيئات الماء المتكونة.